Mestring af konverteringsfaktorer i kemiske formler:En praktisk vejledning
I kemi repræsenterer subscripts i formler kvantitative forhold, ikke kun symboler. Hvert subscript koder for en konverteringsfaktor, der forbinder elementer, molekyler og målbare mængder. At forstå disse skjulte multiplikatorer – ofte kaldet dimensionsanalyse – er afgørende for nøjagtige beregninger inden for støkiometri, laboratoriearbejde og kemiteknik.
Moler af forbindelser til mol af grundstoffer
I en kemisk formel angiver et heltal, hvor mange mol af det foregående element (eller gruppe) der er til stede pr. mol af forbindelsen. For eksempel indeholder vand (H2O) to mol hydrogen og et mol oxygen pr. mol H2O. De tilsvarende konverteringsfaktorer er:
- 2 molH / 1 molH2O
- 1 molO / 1 molH2O
Moler til atomer og molekyler
Et mol er defineret som 6,022×10²³ enheder – atomer, ioner eller molekyler. Omregningsfaktoren er derfor:
- 6,022×10²³atomer (eller molekyler) / 1mol
Muldvarp til gram
Gram giver en målbar masse i laboratoriet. Omregningsfaktoren for et grundstof kommer fra dets atommasse (normalt angivet under symbolet i det periodiske system). For eksempel har germanium en atommasse på 72,61 gmol⁻¹, så:
- 72,61gGe / 1molGe
Procentandele til muldvarp
Nogle formler indeholder brøkdele, der repræsenterer vægt- eller molprocenter i stedet for hele tal. For at konvertere en procentbaseret sammensætning til hele talsabonnementer skal du dividere 100 % med den mindste procentværdi og derefter gange hver procentdel med denne faktor. Eksempel:for C0.₂H0.₆O0.₂ er den mindste procent 20%. At dividere 100 med 20 giver 5. Multiplicering af hver procentdel med 5 giver den forenklede formel CH₃O.
At mestre disse konverteringsfaktorer udstyrer dig med den præcision, der er nødvendig for støkiometriske beregninger, materialebalance og analytisk kemi.
 Varme artikler
Varme artikler
-
 På linjen:At se nanopartikler komme i formKredit:Lawrence Berkeley National Laboratory Flydende strukturer - flydende dråber, der bevarer en bestemt form - er nyttige til en række forskellige anvendelser, fra fødevareforarbejdning til kos
På linjen:At se nanopartikler komme i formKredit:Lawrence Berkeley National Laboratory Flydende strukturer - flydende dråber, der bevarer en bestemt form - er nyttige til en række forskellige anvendelser, fra fødevareforarbejdning til kos -
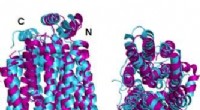 Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry
Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry -
 Selvstændig samling i flere trin åbner døren til nye rekonfigurerbare materialerMaterialevidenskab og ingeniørprofessor Qian Chen, centrum, og kandidatstuderende Binbin Luo, venstre, og Ahyoung Kim finder inspiration i biologi til at hjælpe med at undersøge, hvordan orden stammer
Selvstændig samling i flere trin åbner døren til nye rekonfigurerbare materialerMaterialevidenskab og ingeniørprofessor Qian Chen, centrum, og kandidatstuderende Binbin Luo, venstre, og Ahyoung Kim finder inspiration i biologi til at hjælpe med at undersøge, hvordan orden stammer -
 Bundlemere (nye polymerenheder) kunne transformere industrierEn formel kaldet Thiol-Michael Reaction til konjugering af peptider. Kredit:Kathy F. Atkinson Fra dæk til tøj til shampoo, mange allestedsnærværende produkter fremstilles med polymerer, store kæde
Bundlemere (nye polymerenheder) kunne transformere industrierEn formel kaldet Thiol-Michael Reaction til konjugering af peptider. Kredit:Kathy F. Atkinson Fra dæk til tøj til shampoo, mange allestedsnærværende produkter fremstilles med polymerer, store kæde
- Hvornår forekommer respiration i planter?
- Hvordan er levende organismer afhængige af soi, der lever i vand, der er helt uafhængig af jord so…
- Når et stykke ler falder fra bordet til gulvet, hvad sker der for den potentielle energi, det havde…
- Hvilket enzym findes sandsynligvis i en organisme, der lever de kogende farvande i en dybhavs -termi…
- Iltladning:Forståelse af elektronegativitet og binding
- Hvad sker der, når 2 tektoniske plader spreder sig fra hinanden?


