Hvordan man tegner isomerer:En praktisk trin-for-trin-vejledning
Isomerer er molekyler, der deler den samme molekylære formel, men adskiller sig i arrangementet af deres atomer. At forstå, hvordan man skitserer disse strukturer, er afgørende for kemikere, studerende og alle, der arbejder med organiske forbindelser. Denne guide fører dig gennem hele processen – fra at tælle atomer til at tilføje grene – samtidig med at du sikrer, at hvert atom opfylder dets valenskrav.
Trin 1:Bestem den molekylære formel
Tæl hvert atom i forbindelsen. Den resulterende formel (f.eks. C4H10 ) garanterer, at hver isomer, du tegner, vil indeholde det samme antal af hvert element.
Trin 2:Kend Valence-reglerne
Se det periodiske system eller IUPAC retningslinjer for at finde hvert elements typiske valens:
- H – 1 binding
- C – 4 bindinger
- N – 3 bindinger (ofte 5 i nitriler)
- O – 2 bindinger
- Cl, Br, I – 1 binding
Disse er generelle regler; avanceret binding kan variere (f.eks. hypervalente atomer).
Trin 3:Planlæg rygraden
Vælg grundstoffet med den højeste valens (normalt kulstof). Arranger disse atomer lineært, nummerer dem fra venstre mod højre (1, 2, 3, …). For C4H10 , rygraden er C–C–C–C .
Trin 4:Bekræft antallet af obligationer i rygraden
Tæl de bindinger, som hvert rygradatom har i øjeblikket. For en kæde på fire carbonatomer har de indre carbonatomer hver to bindinger, mens enderne har en. Registrer disse tæller for at vejlede efterfølgende tilføjelser.
Trin 5:Tilføj resterende elementer
Indfør atomer, der kræver færre bindinger (f.eks. brint). Fastgør hver til rygraden, således at hvert atom når sin valens. Placer hydrogener over, under eller ved siden af rygraden for at holde diagrammet læsbart.
Trin 6:Gennemfør den første isomer
Fortsæt med at tilføje hydrogener, indtil alle kulstoffer opfylder deres valens. For C4H10 , dette giver den ligekædede isomer (n-butan). Bekræft, at det samlede antal af hvert element stemmer overens med molekylformlen.
Trin 7:Opret en forgrenet isomer
Start en ny tegning. Behold rygraden, men indfør en gren:
- Fjern det sidste kulstof i kæden (nu er der tre tilbage).
- Føj det fjerde kulstof til det andet kulstof i stedet for det tredje.
- Tjek valens igen:Det andet kulstof har nu tre bindinger (to til naboerne og en til grenen).
- Fyld resterende valenser med hydrogener.
Resultatet er en forgrenet isomer (2-butanons skeletstruktur til illustration). Bekræft atomantal igen.
Trin 8:Generer yderligere isomerer
Gentag forgreningsprocessen på forskellige positioner, eller opret flere forgreninger. For molekyler med mere end to kulstoftyper skal du prioritere at tilføje atomer med den højeste valens først og derefter gå til lavere valenser.
Ting påkrævet
- Blyant (helst HB for nem sletning)
- Papir (almindeligt eller grafisk)
- Lineal (valgfrit, for pænhed)
TL;DR
Isomerer er strukturelle varianter, der deler en molekylær formel. Start med at tælle atomer, følg valensregler, byg en rygrad, og tilføj derefter grene. Brug en blyant og papir til hurtige skitser, eller skift til bold-og-pind-modeller til 3D-visualisering.
Advarsler og avancerede bemærkninger
- Valenceregler er retningslinjer; nogle grundstoffer (f.eks. fosfor, svovl) kan overskride typiske valenser. Undersøg orbitalteori for disse tilfælde.
- Spejlbilleder eller vendte strukturer, der er identiske, er ikke distinkte isomerer. Brug nummerering til at kontrollere for symmetri.
- Ringsystemer indfører yderligere begrænsninger (f.eks. ringstamme). Behersk ligekædede og forgrenede isomerer, før du tackler cykliske strukturer.
For yderligere læsning, se ACS Publications eller IUPAC Compendium of Chemical Terminology .
 Varme artikler
Varme artikler
-
 Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak
Havmuslinger er en model til forbedring af styrke, strækbarhed og vedhæftning i hydrogeler til så…Kredit:Pixabay/CC0 Public Domain Hydrogeler er overalt. De er vandelskende polymerer, der kan absorbere og tilbageholde vand, og kan findes i sådanne dagligdags forbrugerprodukter som bløde kontak -
 Hvordan ioniske forbindelser opløses i vand - Videnskaben bag opløselighed og elektrolytterAf Chris Deziel Opdateret 24. marts 2022 Neznam/iStock/GettyImages I kemi består en ionforbindelse af modsat ladede ioner, der holdes sammen i et krystallinsk gitter. Natriumchlorid (NaCl), dagligd
Hvordan ioniske forbindelser opløses i vand - Videnskaben bag opløselighed og elektrolytterAf Chris Deziel Opdateret 24. marts 2022 Neznam/iStock/GettyImages I kemi består en ionforbindelse af modsat ladede ioner, der holdes sammen i et krystallinsk gitter. Natriumchlorid (NaCl), dagligd -
 Ny metode til at bekæmpe kræft med molekylære fibreKræftcellernes fysiske strukturer forstyrres af en bane, der danner indersiden af cellerne - hvilket aktiverer deres selvdestruktionsmekanisme. Kredit:MPI-P Ifølge Tysklands forbundsstatistiske
Ny metode til at bekæmpe kræft med molekylære fibreKræftcellernes fysiske strukturer forstyrres af en bane, der danner indersiden af cellerne - hvilket aktiverer deres selvdestruktionsmekanisme. Kredit:MPI-P Ifølge Tysklands forbundsstatistiske -
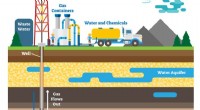 Mekanisme ansvarlig for at skabe halogenerede organiske forbindelser i fracking opdagetForskning fra Kim Parkers laboratorium har fastslået, at tilstedeværelsen af halogenradikaler er en nøgle til dannelsen af halogenerede organiske forbindelser, som er farlige for menneskers sundhe
Mekanisme ansvarlig for at skabe halogenerede organiske forbindelser i fracking opdagetForskning fra Kim Parkers laboratorium har fastslået, at tilstedeværelsen af halogenradikaler er en nøgle til dannelsen af halogenerede organiske forbindelser, som er farlige for menneskers sundhe
- Oxidation vs. Reduktion:Forståelse af kemiske reaktioner
- Forskere opdager, hvordan flere RNA-elementer styrer mikroRNA-biogenese
- Kina siger, at nogle fabrikker har overtrådt anti-smog-foranstaltninger
- Hvad er varmere kerne eller solen?
- Kræfter forekommer altid i lige men overfor hvad?
- Hack får store apps til at vise et antisemitisk navn


