Atombinding:Hvornår danner atomer bindinger?
Her er hvorfor:
* Ædelgasser: Ædelgasserne (helium, neon, argon, krypton, xenon, radon) er meget stabile alene. De har en fuld ydre skal af elektroner, hvilket gør dem meget ureaktive. De danner ikke let bindinger med andre atomer.
* Fri radikaler: Nogle atomer kan eksistere som enkelte, uparrede enheder kaldet frie radikaler. Disse atomer har en uparret elektron i deres ydre skal, hvilket gør dem meget reaktive. Men de danner ikke altid bindinger med andre atomer, især hvis de er meget ustabile og kortlivede.
* Plasma: I en plasmatilstand (en overophedet gas) kan atomer strippes for deres elektroner, hvilket resulterer i en blanding af ioner og elektroner. Selvom disse ladede partikler kan interagere, danner de ikke nødvendigvis traditionelle kemiske bindinger.
Det er mere præcist at sige, at atomer *har tendens* til at binde sig til andre atomer for at opnå stabilitet. Det gør de normalt ved at vinde, miste eller dele elektroner for at fylde deres ydre elektronskaller. Dette er grundlaget for kemisk binding og dannelsen af molekyler.
 Varme artikler
Varme artikler
-
 Sådan kombineres kemiske ligninger:En trin-for-trin guideAf Sean Lancaster Opdateret 30. august 2022 AlexRaths/iStock/GettyImages Kemiske ligninger er kemiens sprog - de beskriver, hvordan stoffer transformeres under en reaktion. For ligetil transformati
Sådan kombineres kemiske ligninger:En trin-for-trin guideAf Sean Lancaster Opdateret 30. august 2022 AlexRaths/iStock/GettyImages Kemiske ligninger er kemiens sprog - de beskriver, hvordan stoffer transformeres under en reaktion. For ligetil transformati -
 Leder efter skjulte tilstande af COVID-19 spike-proteinetAtomisk model til binding af SARS-CoV-2 S-proteinet til ACE2-receptoren på værtscellemembranen. Kredit:University of California, Berkeleky; Istanbuls tekniske universitet Den virus, der skaber kao
Leder efter skjulte tilstande af COVID-19 spike-proteinetAtomisk model til binding af SARS-CoV-2 S-proteinet til ACE2-receptoren på værtscellemembranen. Kredit:University of California, Berkeleky; Istanbuls tekniske universitet Den virus, der skaber kao -
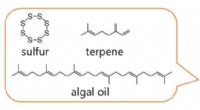 Algeinspirerede polymerer lyser vejen for forbedret nattesynForskere fra University of Tsukuba syntetiserer en elastisk polymer fra billige, bæredygtige materialer, der kan bruges til at fremstille linser, der hjælper med at holde infrarøde kameraer fokuseret
Algeinspirerede polymerer lyser vejen for forbedret nattesynForskere fra University of Tsukuba syntetiserer en elastisk polymer fra billige, bæredygtige materialer, der kan bruges til at fremstille linser, der hjælper med at holde infrarøde kameraer fokuseret -
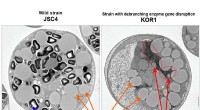 Ændring af kulhydrater til lipider til mikroalger biobrændstofferFigur 1:Elektronmikroskopbillede af lipidproduktion i mikroalgerne Chlamydomonas sp. Kredit:Kobe University Et tværinstitutionelt samarbejde har udviklet en teknik til at fordele kulstofressourcer
Ændring af kulhydrater til lipider til mikroalger biobrændstofferFigur 1:Elektronmikroskopbillede af lipidproduktion i mikroalgerne Chlamydomonas sp. Kredit:Kobe University Et tværinstitutionelt samarbejde har udviklet en teknik til at fordele kulstofressourcer
- Hvordan kan kemiske egenskaber af et stof bestemmes?
- hvilken fysisk egenskab udnyttes ved adskillelse af vand og eddike?
- Planeten, der har massive støvstorme?
- Astronomer ser mærkelige, bue-lignende struktur i Venus-atmosfæren
- Sådan vinder du kundeafhoppere tilbage
- Hvorfor er joviske planeter langt væk fra solen?


