Forståelse af pH af KH2PO4:En detaljeret forklaring
* KH2PO4 er et salt, ikke en stærk syre eller base. Det er dannet ud fra reaktionen mellem en svag syre (H3PO4, fosforsyre) og en stærk base (KOH, kaliumhydroxid).
* Ph-værdien af en saltopløsning afhænger af de relative styrker af syren og basen, der dannede den. I dette tilfælde, da H3PO4 er en svag syre, og KOH er en stærk base, vil opløsningen af KH2PO4 være let sur.
* PH afhænger også af koncentrationen af KH2PO4-opløsningen.
For at bestemme pH-værdien af en KH2PO4-opløsning skal du:
1. Kend koncentrationen af opløsningen.
2. Brug de relevante ligevægtskonstanter: Du skal bruge Ka-værdierne for dissociationen af H3PO4 for at beregne hydrogenionkoncentrationen ([H+]) i opløsningen.
Her er en forenklet forklaring:
KH2PO4 i vand vil delvist dissociere:
KH2PO4(aq) ⇌ K+(aq) + H2PO4-(aq)
H2PO4-ionen kan fungere som både en syre og en base, men det er en svagere syre, end den er en base. Det betyder, at opløsningen vil have en lidt højere koncentration af H+ ioner end OH- ioner, hvilket resulterer i en pH under 7.
For at få en præcis pH-værdi skal du udføre en beregning ved hjælp af de passende ligevægtskonstanter og koncentrationen af KH2PO4-opløsningen.
 Varme artikler
Varme artikler
-
 Kemikere gør historisk fluorfundKredit:University of Texas i San Antonio En banebrydende opdagelse af kemikere ved University of Texas i San Antonio (UTSA) vil have en betydelig indvirkning på, hvordan medicinalvirksomheder udvi
Kemikere gør historisk fluorfundKredit:University of Texas i San Antonio En banebrydende opdagelse af kemikere ved University of Texas i San Antonio (UTSA) vil have en betydelig indvirkning på, hvordan medicinalvirksomheder udvi -
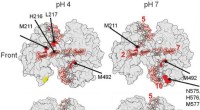 Undersøgelse afslører, hvordan iltfattigt protein binder løst til et mineralud på disse 3-D strukturelle gengivelser af proteinet, hjulpet forskere med at identificere, hvor proteinet binder til et mineral. De røde områder angiver mulige bindingsområder. Kredit:Berkeley Lab
Undersøgelse afslører, hvordan iltfattigt protein binder løst til et mineralud på disse 3-D strukturelle gengivelser af proteinet, hjulpet forskere med at identificere, hvor proteinet binder til et mineral. De røde områder angiver mulige bindingsområder. Kredit:Berkeley Lab -
 Mange små forskelle bidrager til en stor variationEt stof kan påvirke mennesker meget forskelligt. Kredit:Colourbox Der er ikke en enkelt hovedårsag til, at visse stoffer påvirker mennesker forskelligt, men derimod mange små faktorer. ETH-forsker
Mange små forskelle bidrager til en stor variationEt stof kan påvirke mennesker meget forskelligt. Kredit:Colourbox Der er ikke en enkelt hovedårsag til, at visse stoffer påvirker mennesker forskelligt, men derimod mange små faktorer. ETH-forsker -
 Gødning gør drikkevand? En usandsynlig løsning på en global kriseYi Zheng, lektor i maskin- og industriteknik ved Northeastern, har et prøveafsaltningsfilter lavet af kogødning og et lavet af gedehamsereder i sit laboratorium i Mugar Life Sciences Building. Kredit:
Gødning gør drikkevand? En usandsynlig løsning på en global kriseYi Zheng, lektor i maskin- og industriteknik ved Northeastern, har et prøveafsaltningsfilter lavet af kogødning og et lavet af gedehamsereder i sit laboratorium i Mugar Life Sciences Building. Kredit:
- Kvantovergang får elektroner til at opføre sig som om de mangler spin
- Stærkt jordskælv skader 2, slår tagsten af i Japan
- Kan koraller redde vores have? Forskere opdager, at blødt væv kan hjælpe med at beskytte rev
- Hvad er definitionen af emne substantiv?
- Hvad er en femte slags sag?
- Kvantenøgledistributionsnetværk måler nøjagtigt jordvibrationer


