Kemikere gør historisk fluorfund

Kredit:University of Texas i San Antonio
En banebrydende opdagelse af kemikere ved University of Texas i San Antonio (UTSA) vil have en betydelig indvirkning på, hvordan medicinalvirksomheder udvikler nye lægemiddelbehandlinger. Gennembruddet involverer fluor, som danner den næststærkeste kulstofbinding (C-F) kendt for videnskaben, efter carbon-silicium (C-Si) bindingen.
Fluor er et af de mest grundlæggende elementer i livet. I sin fluorform, det er et mineral med anti-syre egenskaber, der bruges i tandpasta og drikkevand for at forhindre tandhuller. Denne lille, ikke-toksisk element bruges også meget af medicinske kemikere i kræftbehandling, antibiotika, antidepressiva, steroider og andre lægemidler. Fluor er udbredt i moderne lægemidler, fordi det stabiliserer lægemidler og forbedrer deres biologiske aktivitet.
I mange år, forskere i UTSA Metalloprotein Research Laboratory, ledet af Aimin Liu, en fremragende Lutcher Brown -professor, har studeret regulering af thioler, forbindelser, der påvirker en række biologiske funktioner hos pattedyr, såsom redox -stressniveauer, energibalance, cellulær signalering, hjertesundhed, og autoimmune og neurologiske tilstande. Når thiolniveauerne er stabile, individer er generelt raske. Når de stiger for meget og for længe, tilstande såsom leddegigt, brystkræft, Alzheimers og Parkinsons sygdomme kan udvikle sig.
Cysteindioxygenase (CDO) og cysteamindioxygenase (ADO) regulerer kroppens thiolniveauer. Når thiolniveauerne er forhøjede, CDO og ADO udvikler katalytiske forstærkere til hurtigt at fjerne thiol fra kroppen. Forskere ved endnu ikke præcist, hvordan enzymerne laver forstærkerne. UTSA -forskerne studerede dette, da de gjorde deres betydelige opdagelse.
Forskerne udførte en teknik på CDO kaldet genetisk kodeudvidelse. Den banebrydende teknik blev bragt til UTSA af post-doktorand Jiasong Li, og blev oprindeligt opfundet af Peter G. Schultz -laboratoriet ved The Scripps Research Institute.
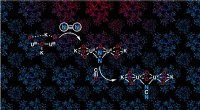
Forskerne skabte en ny form for CDO med to meget stærke carbon-fluorbindinger. Dette burde have gjort det vanskeligere for enzymet at bryde disse carbon-fluor-bindinger og producere dets katalytiske forstærker. Hvad de observerede, imidlertid, overrasket dem. De opdagede, at den modificerede CDO stadig var i stand til at bryde sine carbon-fluorbindinger for at generere sin fulde katalytiske samling.
Dette er første gang, at forskere har demonstreret spaltning (brud) af en carbon-fluorbinding gennem oxidation i proteiner. Det betyder, at det kan være muligt, at menneskelige kroppe er i stand til at bryde disse bindinger i de forbrugte lægemidler.
UTSA -forskerne afdækkede også spor om, hvordan thioler genererer deres katalytiske forstærkere, efter at proteinerne er bygget. Deres opdagelse er beskrevet i Naturens kemiske biologi .
"Dette er en vigtig opdagelse. Mere end 20 procent af de farmaceutiske lægemidler indeholder fluor, "sagde Michael Doyle, Rita og John Feik Distinguished University Chair in Medicinal Chemistry på UTSA. "På grund af deres styrke, fluor-carbonbindinger modstår normal lægemiddelmetabolisme og kan forlænge lægemidlets gavnlige levetid i kroppen. Fluor i lægemiddelmolekyler kan også øge deres evne til at krydse membranbarrierer og komme ind i celler. At carbon-fluor er stærkt modstandsdygtig over for spaltning er en længe troet på medicinsk kemi. Professor Lius opdagelse ændrer det. "
For at udvide deres opdagelse, Liu -laboratoriet, herunder en tredjeårs UTSA-bachelorstuderende, kandidatstuderende, postdoktorer og to kemikere-Wendell Griffith og Daniel Wherritt-benyttede en lignende tilgang til at bestemme den katalytiske samling af ADO, et søskendeenzym til CDO. Ud over succesfuld identifikation af den katalytiske forstærker i ADO, de opdagede et unikt strukturelt motiv, der forhindrede dets påvisning ved rutinemæssige laboratorieteknikker. Disse resultater er rapporteret i et andet papir, der for nylig blev offentliggjort i Angewandte Chemie , et internationalt kendt kemisk tidsskrift.
"Dr. Lius laboratorium giver de studerende fremragende muligheder for at engagere sig i meget interessante og effektive forskningsprojekter, "sagde Waldemar Gorski, professor og formand for UTSA Institut for Kemi.
Mens fluor bruges i vid udstrækning af medicinske kemikere i lægemiddelbehandlinger, Liu siger, at hans teams opdagelse skal minde lægemiddelvirksomheder om, at fluorkemi er meget kompleks. Selvom det er værdifuldt, han anbefaler, at de fortsætter med forsigtighed, fordi der stadig er meget at lære.
"Vi ser et travlt fra farmaceutiske virksomheder til at få medicin gennem udvikling, i kliniske forsøg og på markedet, "sagde Liu." Denne forskning minder os om, at vi skal være grundige og forsigtige. Fluorkemi er meget kompleks. "
"Denne forskning er meget vigtig, "sagde Howard Grimes, Midlertidig dekan for College of Sciences ved UTSA. "At forstå C-F-bindingen er afgørende for vores forståelse af lægemiddeldesign og forbedring af patienters liv."
Sidste artikelNyt gennembrud i krigen mod antibiotikaresistens
Næste artikelKemikere syntetiserer ultrahurtig cyaniddetektor
 Varme artikler
Varme artikler
-
 Isopropanol Alkohol Vs. IsopropylalkoholIsopropylalkohol - også kendt som isopropanol - er almindeligt kendt som gnidning af alkohol. Typisk blandes isopropylalkohol solgt til forbrugerbrug med vand og sælges som en antiseptisk eller ren
Isopropanol Alkohol Vs. IsopropylalkoholIsopropylalkohol - også kendt som isopropanol - er almindeligt kendt som gnidning af alkohol. Typisk blandes isopropylalkohol solgt til forbrugerbrug med vand og sælges som en antiseptisk eller ren -
 Hvordan man laver en 3D-model af en TyphoonTyphoons er tropiske cykloner, der kun findes i det nordvestlige Stillehav. Ligesom orkaner er de lavtrykssystemer med overfladekonvektionsvindestrømme, som er cykloniske. Tyfon og orkan er regionale
Hvordan man laver en 3D-model af en TyphoonTyphoons er tropiske cykloner, der kun findes i det nordvestlige Stillehav. Ligesom orkaner er de lavtrykssystemer med overfladekonvektionsvindestrømme, som er cykloniske. Tyfon og orkan er regionale -
 Nitrogenfiksering under omgivende forholdDen oxo-broforbundne uranforbindelse fanger dinitrogen og omdanner dinitrogen og kulilte til cyanamid. Kredit:Marta Falcone/Marinella Mazzanti/EPFL Rigelig i atmosfæren, kvælstof bruges sjældent t
Nitrogenfiksering under omgivende forholdDen oxo-broforbundne uranforbindelse fanger dinitrogen og omdanner dinitrogen og kulilte til cyanamid. Kredit:Marta Falcone/Marinella Mazzanti/EPFL Rigelig i atmosfæren, kvælstof bruges sjældent t -
 Forskere finder frustration i batterimaterialerKunstnergengivelse af det faste elektrolytmateriale, viser lithium-atomer (lilla) bevæger sig inden for en matrix af anioner sammensat af bor (grøn), kulstof (grå) og brint (hvid) atomer. Kredit:Joel
Forskere finder frustration i batterimaterialerKunstnergengivelse af det faste elektrolytmateriale, viser lithium-atomer (lilla) bevæger sig inden for en matrix af anioner sammensat af bor (grøn), kulstof (grå) og brint (hvid) atomer. Kredit:Joel
- Elbilproducenter bejler til kinesiske købere med rækkevidde, funktioner
- Googles robot lærer at gå i den virkelige verden
- Fejljusteringer i indkapslet grafen fører til kraftig modifikation af elektroniske egenskaber
- Fordelene ved seriel fortynning
- Praktiske anvendelser af destillation
- Bilproducenter søger at elektrificere biludstillingen i Genève, bekæmpe dysterhed


