Dissociation af ionforbindelser:Forståelse af iondannelse
Her er en oversigt:
* Ioniske forbindelser: Disse dannes af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* Dissociation: Dette er den proces, hvor en ionisk forbindelse nedbrydes til dens bestanddele, når den opløses i et opløsningsmiddel, normalt vand.
Sådan fungerer det:
1. Polær opløsningsmiddel: Vandmolekyler er polære, hvilket betyder, at de har en positiv og en negativ ende.
2. Attraktion: Den positive ende af vandmolekyler tiltrækker de negativt ladede anioner af den ioniske forbindelse, og den negative ende tiltrækker de positivt ladede kationer.
3. Adskillelse: Denne tiltrækning er stærk nok til at overvinde de elektrostatiske kræfter, der holder ionerne sammen i det faste krystalgitter.
4. Ioner i løsning: Ionerne er derefter omgivet af vandmolekyler (hydrering), som effektivt adskiller dem fra hinanden og lader dem bevæge sig frit i opløsningen.
Eksempel:
Når bordsalt (NaCl) opløses i vand, opløses det i natriumioner (Na+) og chloridioner (Cl-):
```
NaCl(s) → Na+(aq) + Cl-(aq)
```
Nøglepunkter:
* Dissociation er en vigtig proces i mange kemiske reaktioner og biologiske processer.
* Omfanget af dissociation afhænger af opløseligheden af den ioniske forbindelse i opløsningsmidlet.
* Dissociation er reversibel, hvilket betyder, at ionerne kan rekombinere for at danne den oprindelige ionforbindelse, hvis opløsningsmidlet fjernes.
Sig til, hvis du har yderligere spørgsmål!
Sidste artikelDissociation af ionforbindelser i vand:definition og forklaring
Næste artikelIonic Compound Dissociation:Definition &Process
 Varme artikler
Varme artikler
-
 Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc
Stigning af mandlige individer i stingless bier kolonier fører til dronninger dødUndersøgelse tyder på fremkomsten af hanbier med både faderligt og moderligt genetisk materiale ubalancer arbejdsstyrke i kolonier af Scaptotrigona depilis (fysogastrisk dronning inspicerer yngelc -
 Behov for strenge procedurer inden for elektrokemisk produktion af ammoniakElektrokemisk fremstillet ammoniak. Kredit:Jakob Kibsgaard Ammoniak (NH 3 ) er et af de mest udbredte kemikalier, med en global produktion på 170 megaton om året. Det er nøgleingrediensen i prod
Behov for strenge procedurer inden for elektrokemisk produktion af ammoniakElektrokemisk fremstillet ammoniak. Kredit:Jakob Kibsgaard Ammoniak (NH 3 ) er et af de mest udbredte kemikalier, med en global produktion på 170 megaton om året. Det er nøgleingrediensen i prod -
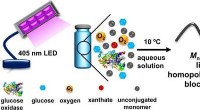 Ultrahøje præcisionspolymererKredit: Angewandte Chemie En miljøvenlig og bæredygtig syntese af tunge polymerer med meget snævre molekylvægtfordelinger er et vigtigt begreb i moderne polymerkemi. Takket være en ny fotoenzymat
Ultrahøje præcisionspolymererKredit: Angewandte Chemie En miljøvenlig og bæredygtig syntese af tunge polymerer med meget snævre molekylvægtfordelinger er et vigtigt begreb i moderne polymerkemi. Takket være en ny fotoenzymat -
 Forskere bruger forskydningskræfter til at skabe selvsamlet supramolekylær hydrogelKemiske strukturer og overblik over geleringsprocessen. Kredit: Naturkemi (2019). DOI:10.1038/s41557-019-0235-8 Et team af forskere ved Southern University of Science and Technology i Kina har fu
Forskere bruger forskydningskræfter til at skabe selvsamlet supramolekylær hydrogelKemiske strukturer og overblik over geleringsprocessen. Kredit: Naturkemi (2019). DOI:10.1038/s41557-019-0235-8 Et team af forskere ved Southern University of Science and Technology i Kina har fu
- Time Machine tilbyder en ny tilgang til lægemiddeltestning af bugspytkirtelkræft
- Slår tornadoer uforholdsmæssigt meget an på trailerparker?
- Superfonde mærker den økonomiske varme fra klimaforandringerne
- Små vandkraftværker gør mere skade end gavn:Modstridende mål i den europæiske miljø- og energi…
- Hvad er den vigtigste opdagelse inden for videnskab?
- Hvad er nogle kommercielle værdier af sedimantariske klipper?


