Time Machine tilbyder en ny tilgang til lægemiddeltestning af bugspytkirtelkræft

Purdue ingeniører byggede en "tidsmaskine, " eller mikrofluidisk bugspytkirteltumoranordning, der simulerer tumorvækst over tid. Kredit:Purdue University/Jared Pike
Mange patienter med kræft i bugspytkirtlen har kun omkring 10 % chance for at overleve inden for fem år efter deres diagnose, fordi de har tendens til at blive resistente over for kemoterapi, tidligere undersøgelser har vist.
En "tidsmaskine", som Purdue Universitys ingeniører har designet til at observere bugspytkirtelkræftadfærd over tid, foreslår en ny tilgang til lægemiddeltestning, der kunne hjælpe videnskabsmænd med bedre at fange resistens.
Forskerne fandt ud af, at testning af potentielle lægemidler på flere tumorcelleundertyper - i stedet for på kun én celleundertype - kan afsløre lægemiddelresistens, der kan opstå på grund af, hvordan forskellige kræftundertyper interagerer med hinanden.
Undersøgelsen blev for nylig offentliggjort i tidsskriftet Royal Society of Chemistry Lab on a Chip .
"Medikamentopdagelsen og -screeningsprocessen har brugt en kræftcelleundertype og studeret, hvordan den interagerer med naboceller, der ikke er kræft, men dette kan overvurdere lægemidlets effektivitet, " sagde Bumsoo Han, en Purdue-professor i maskinteknik og programleder for Purdue Center for Cancer Research. Han har en høflighedsansættelse i biomedicinsk teknik.
"Ved at kondensere tid til at se på, hvordan kræftceller interagerer i en bugspytkirteltumor, vi fandt ud af, at én kræftcelle-undertype ikke kun kan være mere lægemiddelresistent end de andre, men lægemiddelfølsomme celler kan også blive resistente gennem interaktion mellem undertyperne."
"Tidsmaskinen" er en type laboratorieværktøj kaldet en mikrofluidisk enhed. Disse enheder er platforme på størrelse med tyggegummi, såsom en chip eller et objektglas, hvor kræftceller kan dyrkes i kanaler mindre end en millimeter i diameter. Cellerne vokser derefter i et naturtro miljø på platformen, såsom i et kollagenrør, som Hans laboratorium skabte for at efterligne bugspytkirtelkanalen.
Mikrofluidisk udstyr begynder at blive mere mainstream i lægemiddeludviklingsprocessen, fordi de giver forskere mulighed for at teste lægemidler i realistiske simuleringer af et biologisk system ved hjælp af rigtige vævsprøver, men på en hurtigere tidsskala end i dyremodeller.

Denne illustration viser kræftceller, hver celletype repræsenteret af en anden farve, interagerer i kanalerne i en struktur, der efterligner bugspytkirtelkanalen. Kredit:Purdue University/Hye-ran Moon og Altug Ozcelikkale
Hans gruppe fandt, at omkring 25 % af 2019 forskningspublikationer indekseret af PubMed, en biomedicinsk litteraturdatabase, havde brugt mikrofluidiske enheder som modeller til at studere tumorer fra dyr eller patienter.
Men de fleste mikrofluidiske enheder viser kun tumorvækst i det sene stadie. Med Hans enhed, Forskere kan indlæse cellelinjer fra en dyremodel eller patient, før genmutation er sket, gør det muligt for dem at se alle stadier af tumorprogression.
Mens resultater, der er gjort ved hjælp af mikrofluidiske enheder, skal valideres hos mennesker, før de sættes i klinisk praksis, de kan stadig forkorte lægemiddeludviklingsprocessen ved at tilbyde nye forskningstilgange.
Resultaterne fra Hans enhed fremhæver behovet for at studere interaktioner mellem kræftceller.
"Der er ikke blevet forsket meget i, hvilken slags interaktion der sker inden for tumorer, så disse mekanismer for lægemiddelresistens er blevet overset, " sagde Han.
Disse resultater informerer allerede udviklingen af nye lægemiddelforbindelser.
Zhong-Yin Zhang, direktøren for Purdue Institute for Drug Discovery, bruger Hans mikrofluidiske enhed til at teste en forbindelse, der har til formål at blokere en onkogen proces, som Zhangs laboratorium tidligere har identificeret som spiller en rolle i kræftudvikling.
Enheden gør det muligt for Zhangs team at vurdere stoffet ikke kun for specifikt bugspytkirtelkræft, men også på flere kræftcelleundertyper.
"Det gode ved denne enhed er, at vi ikke behøver at bruge så meget af en forbindelse for at se, hvor godt den virker, " sagde Zhang, som også er en fremtrædende professor i medicinsk kemi i Purdues Institut for Medicinalkemi og Molekylær Farmakologi og Institut for Kemi.
 Varme artikler
Varme artikler
-
 Når menneskelig ekspertise forbedrer maskinernes arbejdeGeorgia Tech Ph.D. Kandidat Lee Griffin placerer enkeltkrystalprøven på måletrinnet af det modificerede atomkraftmikroskop (dvs. piezoresponskraftmikroskop). Kredit:Rob Felt, Georgia Tech Maskinlæ
Når menneskelig ekspertise forbedrer maskinernes arbejdeGeorgia Tech Ph.D. Kandidat Lee Griffin placerer enkeltkrystalprøven på måletrinnet af det modificerede atomkraftmikroskop (dvs. piezoresponskraftmikroskop). Kredit:Rob Felt, Georgia Tech Maskinlæ -
 Analytiske metoder hjælper med at udvikle modgift mod cyanid, sennepsgasProfessor Brian Logue, venstre, ser som postdoktoral forskningsassistent Erica Manandhar pipetterer blod i centrifugerør. Kredit:South Dakota State University For at udvikle modgift mod kemiske mi
Analytiske metoder hjælper med at udvikle modgift mod cyanid, sennepsgasProfessor Brian Logue, venstre, ser som postdoktoral forskningsassistent Erica Manandhar pipetterer blod i centrifugerør. Kredit:South Dakota State University For at udvikle modgift mod kemiske mi -
 Video:Vil det kombucha?Kredit:The American Chemical Society Kombucha er en boblende, fermenteret te, der har vundet popularitet i sundheds- og wellness-scenen i løbet af det sidste årti – men hvad er det helt præcist?
Video:Vil det kombucha?Kredit:The American Chemical Society Kombucha er en boblende, fermenteret te, der har vundet popularitet i sundheds- og wellness-scenen i løbet af det sidste årti – men hvad er det helt præcist? -
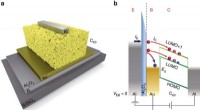 Marcus regime i organiske enheder - grænsefladeladningsoverførselsmekanisme verificeretEnhedsskemaer. a – Skematisk tværsnit af enheden. b – Varmelektrontransistordrift. Elektroner injiceres ved at anvende en negativ emitter-base bias, og detekteret i den molekylære halvleder. Disse ele
Marcus regime i organiske enheder - grænsefladeladningsoverførselsmekanisme verificeretEnhedsskemaer. a – Skematisk tværsnit af enheden. b – Varmelektrontransistordrift. Elektroner injiceres ved at anvende en negativ emitter-base bias, og detekteret i den molekylære halvleder. Disse ele
- Smoky Sydney starter nytårsfester med fyrværkeri
- FN undersøger 35 nordkoreanske cyberangreb i 17 lande
- Uddannelse af journalister i en tid med falske nyheder
- Eschers engle og dæmoner træsnit forudsiger, hvordan stof deformeres
- Forskerhold bruger nanopartikler til at bryde plak op og forhindre hulrum
- Hvorfor klimaforskere ser verdens reaktion på coronavirus


