Forskerhold bruger nanopartikler til at bryde plak op og forhindre hulrum

Lizeng Gao
De bakterier, der lever i tandplak og bidrager til huller i tænderne, modstår ofte traditionel antimikrobiel behandling, da de kan "gemme sig" i en klæbrig biofilmmatrix, et limlignende polymerstillads.
En ny strategi udtænkt af forskere fra University of Pennsylvania tog en mere sofistikeret tilgang. I stedet for blot at påføre et antibiotikum på tænderne, de udnyttede de pH-følsomme og enzymlignende egenskaber af jernholdige nanopartikler til at katalysere aktiviteten af hydrogenperoxid, et almindeligt anvendt naturligt antiseptisk middel. Det aktiverede brintoverilte producerede frie radikaler, der samtidig var i stand til at nedbryde biofilmmatrixen og dræbe bakterierne i, reducerer plak markant og forhindrer huller i tænderne, eller hulrum, i en dyremodel.
"Selv ved at bruge en meget lav koncentration af hydrogenperoxid, processen var utrolig effektiv til at forstyrre biofilmen, " sagde Hyun (Michel) Koo, en professor i Penn School of Dental Medicines afdeling for ortodonti og afdelinger for pædiatrisk tandpleje og samfunds oral sundhed og seniorforfatter af undersøgelsen, som blev offentliggjort i tidsskriftet Biomaterialer . "Tilføjelse af nanopartikler øgede effektiviteten af bakteriedræbende mere end 5, 000 gange."
Avisens hovedforfatter var Lizeng Gao, en postdoc i Koos laboratorium. Medforfattere var Yuan Liu, Dongyeop Kim, Yong Li og Geelsu Hwang, hele Koos laboratorium, samt David Cormode, en assisterende professor i radiologi og bioteknik med ansættelser i Penns Perelman School of Medicine og School of Engineering and Applied Science, og Pratap C. Naha, en postdoc i Cormodes laboratorium.
Værket byggede på et skelsættende fund af Gao og kolleger, udgivet i 2007 i Natur nanoteknologi , viser, at nanopartikler, længe antaget at være biologisk og kemisk inert, kunne faktisk besidde enzymlignende egenskaber. I den undersøgelse Gao viste, at en jernoxidnanopartikel opførte sig på samme måde som en peroxidase, et enzym, der findes naturligt, og som katalyserer oxidative reaktioner, bruger ofte hydrogenperoxid.
Da Gao kom til Koos laboratorium i 2013, han foreslog at bruge disse nanopartikler i orale omgivelser, da oxidationen af brintoverilte producerer frie radikaler, der kan dræbe bakterier.
"Da han først præsenterede det for mig, Jeg var meget skeptisk, " sagde Koo, "fordi disse frie radikaler også kan skade sundt væv. Men så afviste han det og fortalte mig, at det er anderledes, fordi nanopartiklernes aktivitet er afhængig af pH."
Gao havde fundet ud af, at nanopartiklerne ikke havde nogen katalytisk aktivitet ved neutral eller næsten neutral pH på 6,5 eller 7, fysiologiske værdier, der typisk findes i blod eller i en sund mund. Men når pH var sur, tættere på 5, de bliver meget aktive og kan hurtigt producere frie radikaler.
Scenariet var ideelt til målretning af plak, som kan producere et surt mikromiljø, når det udsættes for sukker.
Gao og Koo rakte ud til Cormode, som havde erfaring med at arbejde med jernoxidnanopartikler i en radiologisk billeddannelsessammenhæng, for at hjælpe dem med at syntetisere, karakterisere og teste effektiviteten af nanopartiklerne, hvoraf flere former allerede er FDA-godkendt til billeddannelse hos mennesker.
Begyndende med in vitro undersøgelser, som involverede at dyrke en biofilm indeholdende den hulrumsfremkaldende bakterie Streptococcus mutans på en tandemaljelignende overflade og derefter udsætte den for sukker, forskerne bekræftede, at nanopartiklerne klæbede til biofilmen, blev bibeholdt, selv efter behandlingen var stoppet, og kunne effektivt katalysere hydrogenperoxid under sure forhold.
De viste også, at nanopartiklernes reaktion med en 1 procent eller mindre hydrogenperoxidopløsning var bemærkelsesværdig effektiv til at dræbe bakterier, udslette mere end 99,9 procent af S. mutans i biofilmen inden for fem minutter, en virkning på mere end 5, 000 gange større end at bruge brintoverilte alene. Endnu mere lovende, de viste, at behandlingsregimet, involverer en 30-sekunders topisk behandling af nanopartiklerne efterfulgt af en 30-sekunders behandling med hydrogenperoxid, kunne nedbryde biofilmmatrixkomponenterne, i det væsentlige fjerner det beskyttende klæbrige stillads.
At flytte til en dyremodel, de påførte nanopartiklerne og brintoverilte topisk på tænderne på rotter, som kan udvikle huller i tænderne, når de er inficeret med S. mutans ligesom mennesker gør. To gange om dagen, et minuts behandlinger i tre uger reducerede markant opståen og sværhedsgraden af karieslæsioner, den kliniske betegnelse for huller i tænderne, sammenlignet med kontrollen eller behandlingen med hydrogenperoxid alene. Forskerne observerede ingen negative virkninger på tyggegummi eller orale bløde væv fra behandlingen.
"Det er meget lovende, " sagde Koo. "Effektiviteten og toksiciteten skal valideres i kliniske undersøgelser, men jeg tror, potentialet er der."
Blandt de attraktive funktioner ved platformen er det faktum, at komponenterne er relativt billige.
"Hvis du ser på den mængde, du skal bruge til en dosis, du ser på noget i retning af 5 milligram, " sagde Cormode. "Det er en lille mængde materiale, og nanopartiklerne syntetiseres forholdsvis let, så vi taler om en pris på cents pr. dosis."
Ud over, platformen bruger en koncentration af hydrogenperoxid, 1 procent, hvilket er lavere end mange i øjeblikket tilgængelige tandblegningssystemer, der bruger 3 til 10 procent koncentrationer, minimere risikoen for negative bivirkninger.
Ser frem til, Gao, Koo, Cormode og kolleger håber at fortsætte med at forfine og forbedre effektiviteten af nanopartikelplatformen til at bekæmpe biofilm.
"Vi studerer rollen af nanopartikelbelægninger, sammensætning, størrelse og så videre, så vi kan konstruere partiklerne til endnu bedre ydeevne, " sagde Cormode.
 Varme artikler
Varme artikler
-
 Grafenbaserede diske sikrer sikker opbevaring(Phys.org) —Swinburne University of Technologys forskere har vist potentialet i et nyt materiale til at transformere sikker optisk informationslagring. I deres seneste forskningsartikel offentliggjor
Grafenbaserede diske sikrer sikker opbevaring(Phys.org) —Swinburne University of Technologys forskere har vist potentialet i et nyt materiale til at transformere sikker optisk informationslagring. I deres seneste forskningsartikel offentliggjor -
 Fluorescerende molekyle kunne kaste lys over de indre funktioner i det cellulære miljøSnapshots af det roterende fluorescerende molekyle ved gradvist stigende mikroviskositet viser, hvordan sonden bliver mere og mere udvidet og blottet. Kredit:A*STAR Bioinformatics Institute Et flu
Fluorescerende molekyle kunne kaste lys over de indre funktioner i det cellulære miljøSnapshots af det roterende fluorescerende molekyle ved gradvist stigende mikroviskositet viser, hvordan sonden bliver mere og mere udvidet og blottet. Kredit:A*STAR Bioinformatics Institute Et flu -
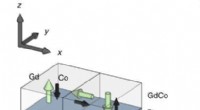 Forskere finder ferrimagneter kunne bruges til at fremskynde spintronics -enhederSkematisk af Pt/Co 44 Gd 56 lagstruktur, hvor ferrimagnetisk Co 44 Gd 56 udviser en vinkelret magnetisk anisotropi (TaO x hætten er ikke vist). Grønne (sorte) pile angiver Gd (Co) sublattice
Forskere finder ferrimagneter kunne bruges til at fremskynde spintronics -enhederSkematisk af Pt/Co 44 Gd 56 lagstruktur, hvor ferrimagnetisk Co 44 Gd 56 udviser en vinkelret magnetisk anisotropi (TaO x hætten er ikke vist). Grønne (sorte) pile angiver Gd (Co) sublattice -
 Forskere kombinerer grafen og kobber i håb om at krympe elektronikPradyumna Goli, venstre, og Alexander Balandin i Balandins Nano-Device Laboratory. (Phys.org)-Forskere har opdaget, at oprettelse af en sandwich med grafen-kobber-grafen stærkt forbedrer kobberens
Forskere kombinerer grafen og kobber i håb om at krympe elektronikPradyumna Goli, venstre, og Alexander Balandin i Balandins Nano-Device Laboratory. (Phys.org)-Forskere har opdaget, at oprettelse af en sandwich med grafen-kobber-grafen stærkt forbedrer kobberens
- Vurdering af virkningen af menneskelig associeret frigivelse af nitrogen til miljøet
- Forbrugerne foretrækker svinekød tilberedt til 145 grader Fahrenheit, siger undersøgelse
- Tegn på tidligere mega-skælv i Californien viser fare for den store på San Andreas-fejl
- Avanceret virtuel teknologi fanger, hvordan koralrev kommer sig efter blegning
- Nanopartikler forbedrer solopsamlingseffektiviteten
- Til hvilken pris? Debatten svirrer om giveaways efter Amazon HQ-aftale


