BCl3-hybridisering:Forståelse af bors geometri (sp²)
1. Tæl antallet af elektrondomæner omkring det centrale atom:
* Bor har 3 valenselektroner.
* Hvert kloratom bidrager med 1 elektron til binding.
* Totale elektrondomæner omkring bor =3 (3 bindinger)
2. Relater antallet af elektrondomæner til hybridiseringen:
* 3 elektrondomæner svarer til sp 2 hybridisering.
Derfor er hybridiseringen af bor i BCl3 sp 2 .
Forklaring:
* I sp 2 hybridisering, en s orbitaler og to p orbitaler af det centrale atom kombineres for at danne tre hybrid orbitaler.
* Disse hybridorbitaler er arrangeret i en trigonal plan geometri, som er formen af BCl3.
Sidste artikelTermisk sammentrækning af metaller:Forståelse af krympning
Næste artikelHybridisering af ClO3-:En trin-for-trin guide
 Varme artikler
Varme artikler
-
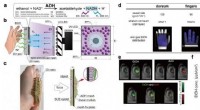 At se det usynlige – Et nyt gasbilleddannelsessystem(a) Detektionsprincip for EtOH baseret på den ADH-medierede katalytiske reaktion. (b) Skematisk diagram af skin-gas-kammen. (c) Arbejdsmekanisme af todimensionel (2D) Mako. (d) Sammenfatning af svedha
At se det usynlige – Et nyt gasbilleddannelsessystem(a) Detektionsprincip for EtOH baseret på den ADH-medierede katalytiske reaktion. (b) Skematisk diagram af skin-gas-kammen. (c) Arbejdsmekanisme af todimensionel (2D) Mako. (d) Sammenfatning af svedha -
 AI fremskynder udviklingen af nye legeringer med høj entropiNye materialer, der anvender AI til at udvikle højentropi-legeringer (HEAer), der er opfundet som legeringer af legeringer. Kredit:Seungchul Lee (POSTECH) Det tager meget tid at udvikle nye materi
AI fremskynder udviklingen af nye legeringer med høj entropiNye materialer, der anvender AI til at udvikle højentropi-legeringer (HEAer), der er opfundet som legeringer af legeringer. Kredit:Seungchul Lee (POSTECH) Det tager meget tid at udvikle nye materi -
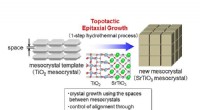 Fotokatalysator gør brintproduktion 10 gange mere effektivSyntese af SrTiOmeso-krystaller ved topotaktisk epitaksial vækst. Kredit:Kobe University Brint er en alternativ energikilde, der kan produceres fra vedvarende kilder til sollys og vand. En gruppe
Fotokatalysator gør brintproduktion 10 gange mere effektivSyntese af SrTiOmeso-krystaller ved topotaktisk epitaksial vækst. Kredit:Kobe University Brint er en alternativ energikilde, der kan produceres fra vedvarende kilder til sollys og vand. En gruppe -
 En præbiotisk vej til DNAKredit:Ludwig Maximilian Universitetet i München DNA kan være dukket op på Jorden tidligere, end man hidtil har antaget. LMU-kemikere ledet af Oliver Trapp viser, at en simpel reaktionsvej kunne h
En præbiotisk vej til DNAKredit:Ludwig Maximilian Universitetet i München DNA kan være dukket op på Jorden tidligere, end man hidtil har antaget. LMU-kemikere ledet af Oliver Trapp viser, at en simpel reaktionsvej kunne h
- Hvad er en kemisk ligning, der beskriver reaktion, der producerer huler i kalksten?
- Hvad rundorme kan lære os om menneskelig vækst
- Hvad er retningen for det elektriske felt modsat den kraft, hvis den er opladet?
- Patenter hjælper med at opbygge et globalt kort over ny rumindustri
- Vildbrande bliver værre over hele kloden. Hvordan sammenligner Californien sig?
- Er aluminium en leder eller isolator?


