Beregning af hexanens kogepunkt ved 1,5 atm:En omfattende vejledning
Forståelse af kogepunkt og tryk
* Kogepunkt: Den temperatur, ved hvilken en væske ændres til en gas.
* Tryk: Den kraft, der udøves pr. arealenhed. Jo højere tryk, jo mere energi kræves der for, at en væske kan overvinde trykket og koge.
Clausius-Clapeyron-ligningen
For at finde kogepunktet for hexan ved et andet tryk, skal du bruge Clausius-Clapeyron-ligningen. Denne ligning relaterer damptrykket af en væske til dens temperatur.
Her er den forenklede form af ligningen:
```
ln(P2/P1) =-ΔHvap/R * (1/T2 - 1/T1)
```
Hvor:
* P1: Væskens damptryk ved temperatur T1 (normalt det normale kogepunkt, som er ved 1 atm).
* P2: Væskens damptryk ved temperatur T2 (det tryk du ønsker at finde kogepunktet ved).
* ΔHvap: Fordampningsentalpien (den mængde energi, der kræves for at fordampe et mol af væsken).
* R: Den ideelle gaskonstant (8,314 J/mol·K).
* T1: Det normale kogepunkt i Kelvin.
* T2: Kogepunktet ved det nye tryk (det du løser for).
Trin til at beregne kogepunktet
1. Find det normale kogepunkt for hexan: Slå det normale kogepunkt for hexan op (ved 1 atm). Det er cirka 69 °C (342 K).
2. Find fordampningsentalpien (ΔHvap): Slå fordampningsentalpien op for hexan. Det er cirka 30,1 kJ/mol.
3. Konverter trykket til de samme enheder: Sørg for, at både P1 og P2 er i de samme trykenheder (f.eks. atm eller kPa).
4. Tilslut værdierne i Clausius-Clapeyron-ligningen:
* P1 =1 atm
* P2 =1,5 atm
* ΔHvap =30,1 kJ/mol (konverter til J/mol:30100 J/mol)
*R =8,314 J/mol·K
* T1 =342 K
* T2 =ukendt
5. Løs for T2: Dette vil være kogepunktet for hexan ved 1,5 atm.
Vigtig bemærkning: Clausius-Clapeyron-ligningen antager ideel gasadfærd, og at fordampningsentalpien er konstant over temperaturområdet. Det er tilnærmelser, så det beregnede kogepunkt vil være et skøn.
 Varme artikler
Varme artikler
-
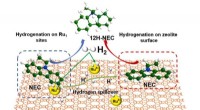 Synergistiske katalysatorer til højeffektiv brintlagringGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121958 Brintenergi betragtes som lovende vedvarende energi. Udviklingen af brintenergi er imidlertid begrænset
Synergistiske katalysatorer til højeffektiv brintlagringGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121958 Brintenergi betragtes som lovende vedvarende energi. Udviklingen af brintenergi er imidlertid begrænset -
 Ny metode til isolering af tumorceller kan forbedre kræftforskning og -behandlingLeidong Mao (til venstre), en lektor ved UGA College of Engineering arbejdede sammen med ph.d.-studerende Wujun Zhao om at udvikle en ny enhed, der er i stand til at isolere tumorceller. Kredit:Univer
Ny metode til isolering af tumorceller kan forbedre kræftforskning og -behandlingLeidong Mao (til venstre), en lektor ved UGA College of Engineering arbejdede sammen med ph.d.-studerende Wujun Zhao om at udvikle en ny enhed, der er i stand til at isolere tumorceller. Kredit:Univer -
 Nedbrydningsstatus for moderne polymere museumsartefakter kan klassificeres efter deres lugtKredit:Wiley Åndedrætsanalyse i sygdomsdiagnostik er et lovende forskningsfelt, og fremskridtene inden for instrumentering muliggør nøjagtig påvisning af metabolitter. Men ikke kun patienternes he
Nedbrydningsstatus for moderne polymere museumsartefakter kan klassificeres efter deres lugtKredit:Wiley Åndedrætsanalyse i sygdomsdiagnostik er et lovende forskningsfelt, og fremskridtene inden for instrumentering muliggør nøjagtig påvisning af metabolitter. Men ikke kun patienternes he -
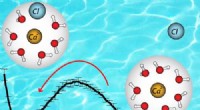 Udforskning af forholdet mellem to-kroppen og kollektivetDen frie energi er forskellig mellem ionparret (venstre) og ionen alene (højre). Det var ikke muligt at se denne forskel med tidligere tilgange. Kredit:American Chemical Society Fra batterier til
Udforskning af forholdet mellem to-kroppen og kollektivetDen frie energi er forskellig mellem ionparret (venstre) og ionen alene (højre). Det var ikke muligt at se denne forskel med tidligere tilgange. Kredit:American Chemical Society Fra batterier til
- Heterofase nanostrukturer, der bidrager til effektiv katalyse
- Udvikling af kvantealgoritmer til optimeringsproblemer
- Hvad afhænger den tilsyneladende bevægelse af genstande i himlen?
- Billeddannelse af turbulens inden for soltransienter for første gang
- Global stigning på 2 grader C fordobler befolkning udsat for flere klimarisici sammenlignet med 1,5…
- Er Obsidian en instruerende eller ekstruderende stødende rock, hvordan ved du det?


