Forståelse af spontane reaktioner ved 298K:Gibbs Free Energy
* ΔG <0: Reaktionen er spontan (eksergonisk)
* ΔG> 0: Reaktionen er ikke-spontan (endergonisk)
* ΔG =0: Reaktionen er i ligevægt
Gibbs Free Energy-ændringen er relateret til entalpiændring (ΔH) og entropiændring (ΔS) ved ligningen:
ΔG =ΔH - TΔS
hvor:
* ΔH er ændringen i entalpi (varme frigivet eller absorberet)
* T er temperaturen i Kelvin
* ΔS er ændringen i entropi (uorden eller tilfældighed)
Derfor kan en spontan reaktion ved 298 K forekomme i følgende scenarier:
1. Eksoterm reaktion (ΔH <0) med en stigning i entropi (ΔS> 0): Dette scenarie resulterer altid i en negativ ΔG, hvilket gør reaktionen spontan.
2. Eksoterm reaktion (ΔH <0) med et lille fald i entropi (ΔS <0): Hvis entalpiændringen er signifikant negativ, kan den overvinde et lille fald i entropi, hvilket fører til en negativ ΔG og en spontan reaktion.
3. Endoterm reaktion (ΔH> 0) med en stor stigning i entropi (ΔS> 0): Hvis entropistigningen er signifikant nok til at opveje den positive entalpiændring, vil reaktionen have en negativ ΔG og være spontan.
Eksempler på spontane reaktioner ved 298 K:
* Forbrænding af brændstoffer: Eksoterm med stor stigning i entropi.
* Opløsning af bordsalt i vand: Endoterm med stor stigning i entropi.
* Neutraliseringsreaktion af en stærk syre med en stærk base: Eksoterm med en lille stigning i entropi.
Bemærk: Spontaniteten af en reaktion kan også påvirkes af faktorer som koncentration, tryk og tilstedeværelsen af katalysatorer.
 Varme artikler
Varme artikler
-
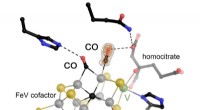 Vanadiumafhængig nitrogenase kan binde to CO-molekyler samtidigtJern-vanadium (FeV) cofaktoren i vanadiumafhængig nitrogenase blev lavet til at reagere med carbonmonoxid (CO) og derefter gasset under tryk, tillader to molekyler af substratet at blive visualiseret
Vanadiumafhængig nitrogenase kan binde to CO-molekyler samtidigtJern-vanadium (FeV) cofaktoren i vanadiumafhængig nitrogenase blev lavet til at reagere med carbonmonoxid (CO) og derefter gasset under tryk, tillader to molekyler af substratet at blive visualiseret -
 Forskere kæmper mod udryddelse for at afsløre træers kræftbekæmpende egenskaberEt kinesisk frimærke til ære for det kritisk truede træ blev udstedt i 1992. Kredit:Designet af Zeng Xiaolian Tre kinesiske grantræer på et naturreservat i det sydøstlige Kina er de sidste af dere
Forskere kæmper mod udryddelse for at afsløre træers kræftbekæmpende egenskaberEt kinesisk frimærke til ære for det kritisk truede træ blev udstedt i 1992. Kredit:Designet af Zeng Xiaolian Tre kinesiske grantræer på et naturreservat i det sydøstlige Kina er de sidste af dere -
 Sporing af chiralitet i realtidKunstnerens indtryk af en tidsopløst cirkulær dikroismemåling af et fotoexciteret spin-crossover-kompleks. Kredit:Ella Maru Studio, Inc. Chirale molekyler findes i to former, kaldet enantiomerer, s
Sporing af chiralitet i realtidKunstnerens indtryk af en tidsopløst cirkulær dikroismemåling af et fotoexciteret spin-crossover-kompleks. Kredit:Ella Maru Studio, Inc. Chirale molekyler findes i to former, kaldet enantiomerer, s -
 Lab afslører hjerte-på-en-chipGennem hjerte-på-en-chip-teknologi - modellering af et menneskeligt hjerte på en konstrueret chip og måling af virkningerne af forbindelseseksponering ved hjælp af mikroelektroder - håber Lawrence Liv
Lab afslører hjerte-på-en-chipGennem hjerte-på-en-chip-teknologi - modellering af et menneskeligt hjerte på en konstrueret chip og måling af virkningerne af forbindelseseksponering ved hjælp af mikroelektroder - håber Lawrence Liv
- Oprettelse og selektiv funktionalisering af viruslignende polymerpartikler
- Amazon er muligvis klar til at tage imod Apples AirPods, siger rapporten
- Hvilke stjerner er meget seje, men lysende?
- Hvilken type landform dannes af en mantelplume?
- Afsløring af Triceratops-holdningen:En lidt kendt debat afsløret
- Guldproteinklynger kunne bruges som miljø- og sundhedsdetektorer


