Umættede vs. mættede kulbrinter:egenskaber og forskelle
Umættede vs. mættede kulbrinter:nøgleforskelle
Den vigtigste forskel mellem umættede og mættede kulbrinter ligger i de typer bindinger, der er til stede i deres molekyler.
Mættede kulbrinter:
* Indeholder kun enkeltbindinger mellem carbonatomer. Dette betyder, at hvert kulstofatom er bundet til det maksimalt mulige antal hydrogenatomer.
* Generel formel:CnH2n+2 (hvor 'n' repræsenterer antallet af kulstofatomer)
* Eksempler: Metan (CH4), Ethan (C2H6), Propan (C3H8)
* Egenskaber:
* Generelt mindre reaktiv på grund af fraværet af dobbelt- eller tredobbeltbindinger.
* Har tendens til at være gasser eller væsker ved stuetemperatur.
* Har lavere kogepunkter sammenlignet med umættede kulbrinter med det samme antal kulstofatomer.
Umættede kulbrinter:
* Indeholder mindst én dobbelt- eller tredobbeltbinding mellem carbonatomer. Det betyder, at de har færre brintatomer end mættede kulbrinter med det samme antal kulstofatomer.
* Generel formel:
* Alkener: CnH2n (indeholder en eller flere dobbeltbindinger)
* Alkyner: CnH2n-2 (indeholder en eller flere tripelbindinger)
* Eksempler:
* Alkener: Ethen (C2H4), Propen (C3H6)
* Alkyner: Ethyn (C2H2), Propyn (C3H4)
* Egenskaber:
* Mere reaktiv på grund af tilstedeværelsen af dobbelt- eller tredobbeltbindinger.
* Kan gennemgå additionsreaktioner, hvor dobbelt- eller tredobbeltbindingen brydes og nye atomer tilføjes.
* Har tendens til at have højere kogepunkter sammenlignet med mættede kulbrinter med det samme antal kulstofatomer.
Kort sagt:
* Mættede kulbrinter er "fulde" af hydrogenatomer.
* Umættede kulbrinter har "plads" til flere brintatomer på grund af dobbelt- eller tredobbeltbindingerne.
Denne forskel i binding påvirker de kemiske og fysiske egenskaber af disse forbindelser, hvilket fører til variationer i deres reaktivitet, kogepunkter og anvendelser.
 Varme artikler
Varme artikler
-
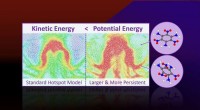 Forskning afdækker manglende fysik i eksplosive hotspotsMolekylær dynamik simuleringer forudsiger, at mere potentiel energi er lokaliseret i hotspots, end deres kinetiske energi (eller temperatur) antyder. Overskydende potentiel energi er bundet til vedvar
Forskning afdækker manglende fysik i eksplosive hotspotsMolekylær dynamik simuleringer forudsiger, at mere potentiel energi er lokaliseret i hotspots, end deres kinetiske energi (eller temperatur) antyder. Overskydende potentiel energi er bundet til vedvar -
 Opdagelse kan fjerne mikropollutanter fra miljøetDr. Rong Ye (til venstre), Dr. Ming Zhao (i midten), og Dr. Peng Cheng (til højre) i Cornell diskuterer deres hærfinansierede forskning, der identificerer en ny kemitilgang, der kan fjerne mikropollut
Opdagelse kan fjerne mikropollutanter fra miljøetDr. Rong Ye (til venstre), Dr. Ming Zhao (i midten), og Dr. Peng Cheng (til højre) i Cornell diskuterer deres hærfinansierede forskning, der identificerer en ny kemitilgang, der kan fjerne mikropollut -
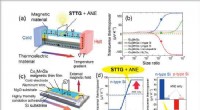 Demonstration af ukonventionel tværgående termoelektrisk generationFigur. (a) Skematisk diagram, der viser begrebet Seebeck-drevet tværgående termoelektrisk generation (STTG). Ladestrømmen forårsaget af Seebeck -effekten i det termoelektriske materiale genererer en s
Demonstration af ukonventionel tværgående termoelektrisk generationFigur. (a) Skematisk diagram, der viser begrebet Seebeck-drevet tværgående termoelektrisk generation (STTG). Ladestrømmen forårsaget af Seebeck -effekten i det termoelektriske materiale genererer en s -
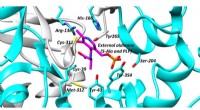 Forskere udforsker racemaser og foreslår strategier til at finde lægemidler, der er målrettet mod…Det aktive sted for alanin racemase, et vigtigt antibakterielt mål. Kredit:University of Bath Forskere fra Storbritanniens University of Bath udforsker racemaser-en vigtig type enzym, der er knytt
Forskere udforsker racemaser og foreslår strategier til at finde lægemidler, der er målrettet mod…Det aktive sted for alanin racemase, et vigtigt antibakterielt mål. Kredit:University of Bath Forskere fra Storbritanniens University of Bath udforsker racemaser-en vigtig type enzym, der er knytt
- Sådan konverteres Kilojoules til Kilocalories
- Hvordan vil vi kolonisere andre planeter?
- Kan en krop have acceleration, mens du er i hvile?
- Processen med at opdele mad i molekyler kan kroppen bruge?
- Hvilke grundstoffer reagerer med saltsyre? En praktisk guide
- Goldilocks influencers:Hvorfor et højt antal følgere måske ikke er den bedste drivkraft for engag…


