Kovalente bindinger:Når elektronegativitetsforskelle er små
Her er hvorfor:
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding.
* Kovalent binding: Denne type binding opstår, når atomer deler elektroner.
Når elektronegativitetsforskellen er lille, har ingen af atomerne et væsentligt stærkere træk på de delte elektroner. Dette betyder, at de vil blive delt relativt ligeligt, hvilket fører til en kovalent binding.
Eksempel:
* Oxygen (O) og klor (Cl): De har lignende elektronegativitetsværdier, hvilket resulterer i en kovalent binding i molekylet Cl2O .
Vigtig bemærkning:
* En meget lille elektronegativitetsforskel kan nogle gange resultere i en polær kovalent binding . Det betyder, at elektronerne stadig deles, men ikke helt ligeligt. Et atom vil have et lidt stærkere træk på de delte elektroner, hvilket skaber en let positiv og negativ ladning på molekylet.
* Hvis elektronegativitetsforskellen er stor, en ionisk binding er mere tilbøjelige til at dannes, hvor det ene atom effektivt overfører en elektron til det andet og skaber ioner med modsatte ladninger.
 Varme artikler
Varme artikler
-
 Vurdering af den luftbårne overlevelse af bakterier i aerosoldråber fra hoste og nysVed at bruge den nye tilgang, skyer af aerosoldråber (f.eks. 40 vist på billedet) kan fanges og manipuleres, muliggør en simulering af deres miljøeksponering Kredit:University of Bristol Den luftb
Vurdering af den luftbårne overlevelse af bakterier i aerosoldråber fra hoste og nysVed at bruge den nye tilgang, skyer af aerosoldråber (f.eks. 40 vist på billedet) kan fanges og manipuleres, muliggør en simulering af deres miljøeksponering Kredit:University of Bristol Den luftb -
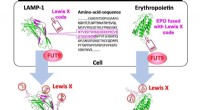 Forskerhold identificerer en molekylær kode indlejret i protein til regulering af dets glykosylerin…Specifik 29-aminosyresekvens fra LAMP-1 tjener som en Lewis X-kode, som dechifreres af FUT9, og den kan indlejres i erythropoietin for at fremkalde Lewis X-modifikation. Kredit:Nagoya City University
Forskerhold identificerer en molekylær kode indlejret i protein til regulering af dets glykosylerin…Specifik 29-aminosyresekvens fra LAMP-1 tjener som en Lewis X-kode, som dechifreres af FUT9, og den kan indlejres i erythropoietin for at fremkalde Lewis X-modifikation. Kredit:Nagoya City University -
 Forskere bruger Theta til analyse i realtid af COVID-19 proteinerNsp10/16 overflade med ligander. Forskere har udviklet en pipeline til at forbinde ALCF-supercomputere med APS-eksperimenter for at muliggøre analyse i realtid af COVID-19-proteiner, baner vejen for a
Forskere bruger Theta til analyse i realtid af COVID-19 proteinerNsp10/16 overflade med ligander. Forskere har udviklet en pipeline til at forbinde ALCF-supercomputere med APS-eksperimenter for at muliggøre analyse i realtid af COVID-19-proteiner, baner vejen for a -
 Nye tilgange til at undersøge de molekylære årsager til amyloiddannelseIllustration af en voksende fibril i fælden og laseren. Kredit:Martin Fränzl Mere end 24 millioner mennesker verden over lider af neurodegenerative sygdomme som Alzheimers, Parkinsons eller Huntin
Nye tilgange til at undersøge de molekylære årsager til amyloiddannelseIllustration af en voksende fibril i fælden og laseren. Kredit:Martin Fränzl Mere end 24 millioner mennesker verden over lider af neurodegenerative sygdomme som Alzheimers, Parkinsons eller Huntin


