Kationer i ionisk binding:Forståelse af metaladfærd
* Metaller har lav elektronegativitet: De har et svagere greb om deres valenselektroner.
* Ikke-metaller har høj elektronegativitet: De har en stærk tiltrækning af elektroner.
Når et metal og et ikke-metal bindes ionisk, *taber* metalatomet en eller flere elektroner for at blive en positivt ladet ion (kation). Ikke-metalatomet *vinder* disse elektroner og bliver til en negativt ladet ion (anion).
Eksempel: I natriumchlorid (NaCl) er natrium (Na) et metal, og chlor (Cl) er et ikke-metal. Natrium mister en elektron for at blive en natriumkation (Na+), mens klor får den elektron til at blive en chloridanion (Cl-). De modsatte ladninger tiltrækker hinanden og danner den ioniske forbindelse.
 Varme artikler
Varme artikler
-
 Forskerhold rekonstruerer motor-lastkompleks til ciliær transportDr. Zeynep Oekten og medforfatter Willi L. Stepp ved det fluorescensmikroskop, de bruger til at observere de motoriske proteiner, der løber langs mikrotubulierne (se video). Kredit:Andreas Battenberg
Forskerhold rekonstruerer motor-lastkompleks til ciliær transportDr. Zeynep Oekten og medforfatter Willi L. Stepp ved det fluorescensmikroskop, de bruger til at observere de motoriske proteiner, der løber langs mikrotubulierne (se video). Kredit:Andreas Battenberg -
 CLOUD ved CERN afslører jodsyrers rolle i atmosfærisk aerosoldannelseSimulering af den marine atmosfære i CLOUD -kammeret. Jod fra havet og is omdannes af ozon og sollys til jodsyre og andre forbindelser. Disse danner nye partikler og øger skyer, opvarmning af polarkli
CLOUD ved CERN afslører jodsyrers rolle i atmosfærisk aerosoldannelseSimulering af den marine atmosfære i CLOUD -kammeret. Jod fra havet og is omdannes af ozon og sollys til jodsyre og andre forbindelser. Disse danner nye partikler og øger skyer, opvarmning af polarkli -
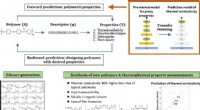 Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM], -
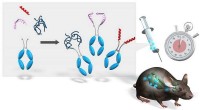 Forskere skaber effektiv semisyntese af biofarmaceutiske-Fc-konjugaterBiopharmaceutic-Fc-konjugat syntetiseret ved vores metode havde en lang halveringstid inde i kroppen. Kredit:University of Electro Communications Biofarmaceutik bestående af mellemmolekyler, for e
Forskere skaber effektiv semisyntese af biofarmaceutiske-Fc-konjugaterBiopharmaceutic-Fc-konjugat syntetiseret ved vores metode havde en lang halveringstid inde i kroppen. Kredit:University of Electro Communications Biofarmaceutik bestående af mellemmolekyler, for e
- Hvad er fordele og ulemper ved flowcytometri?
- Fysikere er banebrydende for ny kvanteregistreringsplatform
- Undersøgelse viser en formindsket, men robust sammenhæng mellem fagforeningsnedgang, stigende ulig…
- Kan månen ses hvor som helst når som helst?
- Infanteritank Mark II A-12
- Hvis der ikke er noget lys gennem dette materiale, er det?


