Ionbinding:Elektronoverførsel og iondannelse forklaret
Det grundlæggende
* Ioniske bindinger opstår mellem et metal og et ikke-metal. Metaller har tendens til at tabe elektroner, mens ikke-metaller har tendens til at få elektroner.
* Elektroner overføres, deles ikke. Dette er en nøgleforskel mellem ioniske og kovalente bindinger.
Processen
1. Metal mister en elektron: Metalatomet, med dets løst fastholdte elektroner, mister en eller flere elektroner. Dette skaber en positivt ladet ion (kaldet en kation).
2. Ikke-metal får en elektron: Det ikke-metaliske atom, med et stærkt ønske om at færdiggøre sin ydre elektronskal, vinder den eller de elektroner, der går tabt af metallet. Dette skaber en negativt ladet ion (kaldet en anion).
3. Elektrostatisk tiltrækning: De modsat ladede ioner tiltrækkes nu af hinanden på grund af elektrostatiske kræfter. Denne tiltrækning er det, der holder ionerne sammen i den ioniske forbindelse.
Eksempel:Natriumchlorid (NaCl)
* Natrium (Na) , et metal, mister en elektron for at blive en natriumion (Na+).
* Klor (Cl) , et ikke-metal, får elektronen til at blive en chloridion (Cl-).
* De modsat ladede ioner (Na+ og Cl-) tiltrækker hinanden, danner en ionbinding og skaber forbindelsen natriumchlorid (NaCl).
Nøglepunkter
* Overførsel af elektroner er det, der definerer ionbinding.
* De resulterende ioner har fulde ydre elektronskaller, hvilket gør dem mere stabile.
* Den stærke elektrostatiske tiltrækning mellem ionerne fører til en forbindelse med et højt smeltepunkt og højt kogepunkt.
Sig til, hvis du vil have flere detaljer eller har andre spørgsmål!
Sidste artikelKationer i ionisk binding:Forståelse af metaladfærd
Næste artikelIonisk binding:Elektrontab, kationdannelse og ladninger
 Varme artikler
Varme artikler
-
 Maskinlæringsværktøj kan hjælpe med at udvikle hårdere materialerKredit:CC0 Public Domain For ingeniører, der udvikler nye materialer eller beskyttende belægninger, der er milliarder af forskellige muligheder for at sortere igennem. Labtest eller endda detaljer
Maskinlæringsværktøj kan hjælpe med at udvikle hårdere materialerKredit:CC0 Public Domain For ingeniører, der udvikler nye materialer eller beskyttende belægninger, der er milliarder af forskellige muligheder for at sortere igennem. Labtest eller endda detaljer -
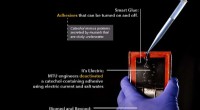 Ingeniører zapper og løsner smart undervandslimTænd og sluk for vedhæftning er det, der gør en lim smart. Det er én ting at gøre dette i det fri og noget helt andet under vand. Inspireret af naturen, katekoler er syntetiske forbindelser, der efter
Ingeniører zapper og løsner smart undervandslimTænd og sluk for vedhæftning er det, der gør en lim smart. Det er én ting at gøre dette i det fri og noget helt andet under vand. Inspireret af naturen, katekoler er syntetiske forbindelser, der efter -
 At se nærmere på genetiske skift i kræftEn krystalstruktur af en del af menneskelig DPF2, et protein, der styrer en genetisk switch, der fortæller blodstamceller, hvornår de skal blive røde og hvide blodlegemer. Orange og gule områder illus
At se nærmere på genetiske skift i kræftEn krystalstruktur af en del af menneskelig DPF2, et protein, der styrer en genetisk switch, der fortæller blodstamceller, hvornår de skal blive røde og hvide blodlegemer. Orange og gule områder illus -
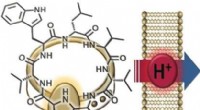 Kemisk syntese viser, at antibiotika fra den menneskelige næse virker ved protontranslokationKredit:Wiley Antibiotika-resistente bakterier er en stigende sundhedstrussel, gør nye antibiotika afgørende. Tyske forskere har for nylig haft et gennembrud:de opdagede lugdunin i den menneskelige
Kemisk syntese viser, at antibiotika fra den menneskelige næse virker ved protontranslokationKredit:Wiley Antibiotika-resistente bakterier er en stigende sundhedstrussel, gør nye antibiotika afgørende. Tyske forskere har for nylig haft et gennembrud:de opdagede lugdunin i den menneskelige
- Hvilken er en sammensat iltheliumkuldioxidnitrogen?
- Forskere opnår kemisk kontrolleret, reversibel magnetisk faseovergang
- Hvad er hovedmålet i træplantning?
- Hvordan er 1750 ml skrevet i liter?
- Vil du opfordre andre til at installere solceller? Handlinger siger mere end ord
- Hvilket sted er på 16 grader nord og 3degrees vest?


