Opløselighed og diffusion:Hvordan faste opløste stoffer opløses
* Overfladeareal: Overfladen af det opløste stof er kontaktpunktet med opløsningsmidlet. Det er her opløsningsmiddelmolekylerne kan interagere med de opløste partikler.
* Diffusion: Når en opløst stof partikel undslipper ind i opløsningsmidlet, kan den diffundere længere ind i opløsningen. Denne diffusionsproces er drevet af koncentrationsgradienten, der bevæger sig fra områder med høj koncentration til områder med lav koncentration.
Det er dog ikke helt korrekt at sige, at partikler KUN slipper ud ved overfladen. Her er hvorfor:
* Intern struktur: Nogle faste stoffer, især dem med defekter eller ufuldkommenheder i deres krystalgitter, kan have nogle opløste partikler, der ikke er tæt bundet i den faste struktur. Disse partikler kan potentielt undslippe ind i opløsningsmidlet inde fra det faste stof.
* Opløsningsproces: Opløsningsprocessen involverer at bryde bindingerne, der holder de opløste partikler sammen og danner nye bindinger med opløsningsmiddelmolekylerne. Denne proces kan forekomme gennem hele det faste stof, selvom det vil være meget hurtigere ved overfladen.
Opsummering: Selvom det er rigtigt, at langt de fleste opløste partikler slipper ud i opløsningsmidlet ved overfladen på grund af overfladeareal og diffusion, er der nogle undtagelser. Opløsningsprocessen kan forekomme i hele det faste stof, men det er betydeligt hurtigere ved overfladen.
 Varme artikler
Varme artikler
-
 Enkel vandtest kunne forhindre lammende knoglesygdomDen enkle test skifter farve fra lilla til blå, når fluorindholdet er for højt. Kredit:University of Bath En enkel farveændrende test for at påvise fluor i drikkevand, udtænkt af forskere ved Univ
Enkel vandtest kunne forhindre lammende knoglesygdomDen enkle test skifter farve fra lilla til blå, når fluorindholdet er for højt. Kredit:University of Bath En enkel farveændrende test for at påvise fluor i drikkevand, udtænkt af forskere ved Univ -
 Forskningsresultater kan reducere energiforbruget og omkostningerne ved fremstilling af siliciumKredit:Curtin University Curtin University forskere har afsløret en metode til fremstilling af silicium, findes almindeligt inden for elektronik såsom telefoner, kameraer og computere, ved stuetem
Forskningsresultater kan reducere energiforbruget og omkostningerne ved fremstilling af siliciumKredit:Curtin University Curtin University forskere har afsløret en metode til fremstilling af silicium, findes almindeligt inden for elektronik såsom telefoner, kameraer og computere, ved stuetem -
 Hvordan man opnår højkrystallinske organisk-uorganiske perovskitfilm til solcellerVed kontakt med to kemiske middelpulvere ved stuetemperatur dannes en tyktflydende mørk væske i løbet af få sekunder. Dette er methylammoniumpolyiodider. Kredit:Alexey Tarasov Medlemmer af Laborat
Hvordan man opnår højkrystallinske organisk-uorganiske perovskitfilm til solcellerVed kontakt med to kemiske middelpulvere ved stuetemperatur dannes en tyktflydende mørk væske i løbet af få sekunder. Dette er methylammoniumpolyiodider. Kredit:Alexey Tarasov Medlemmer af Laborat -
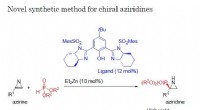 Ny kemisk syntesemetode kan producere en spændende række nye forbindelserForskere ved Nagoya Institute of Technology har etableret en reaktion katalyseret af Bis(imidazolin)/zink, hvorved 2H-aziriner reagerer med phosphit, hvilket giver aziridiner ved et højt enantiomert f
Ny kemisk syntesemetode kan producere en spændende række nye forbindelserForskere ved Nagoya Institute of Technology har etableret en reaktion katalyseret af Bis(imidazolin)/zink, hvorved 2H-aziriner reagerer med phosphit, hvilket giver aziridiner ved et højt enantiomert f
- En lav pris, højeffektiv katalysator, der omdanner kuldioxid til andre kemikalier
- Havbeskyttelsesplan kortlægger kurset for at forsvare Californiens kyst
- Hvad giver den bedste magtkilde til at opretholde livsstøttesystemer i rummet?
- Når du partiklerne gør dette mod stoffer får energi?
- Hvordan planter klarer dagens kolde lys, og hvorfor det betyder noget for fremtidige afgrøder
- Hvilken slags bindinger er komplekse biomolekyler konstrueret af?


