Kobber- og salpetersyrereaktion:en detaljeret forklaring
* Redox-reaktion: Det betyder, at der er en overførsel af elektroner mellem reaktanter. Kobber taber elektroner (oxidation), mens nitrogen i salpetersyre får elektroner (reduktion).
* Enkeltforskydningsreaktion: Kobber fortrænger brint fra salpetersyre, danner kobber(II)nitrat og frigiver nitrogendioxidgas.
Her er den afbalancerede kemiske ligning:
Cu(s) + 4 HNO3(aq) → Cu(NO3)2(aq) + 2 NO2(g) + 2 H2O(l)
Forklaring:
* Kobber (Cu): Det oxideres, mister elektroner og danner kobber(II)-ioner (Cu²⁺).
* Salpetersyre (HNO₃): Nitrogenet i salpetersyre reduceres. Det får elektroner til at danne nitrogendioxidgas (NO₂).
* Kobber(II)nitrat (Cu(NO₃)₂): Dette dannes ved at kobberionerne reagerer med nitrationer fra salpetersyren.
* Nitrogendioxid (NO₂): Dette er en rødbrun gas, der frigives under reaktionen.
* Vand (H₂O): Dette dannes også som et biprodukt af reaktionen.
Vigtig bemærkning: Denne reaktion sker kun med koncentreret salpetersyre. Fortyndet salpetersyre vil reagere med kobber for at producere kobber(II)nitrat og nitrogenoxid (NO) gas i stedet for nitrogendioxid.
Sidste artikelKobber- og salpetersyrereaktion:Forståelse af kemien
Næste artikelZink- og eddikesyrereaktion:Produkt, ligning og forklaring
 Varme artikler
Varme artikler
-
 Fysikstuderende udvikler maskinlæringsmodel til energi- og miljøapplikationerEn fysikstuderende ved West Virginia University har skabt en ny maskinlæringsmodel, der har potentialet til at gøre søgningen efter energi- og miljømaterialer mere effektiv. Gihan Panapitiya, en dokt
Fysikstuderende udvikler maskinlæringsmodel til energi- og miljøapplikationerEn fysikstuderende ved West Virginia University har skabt en ny maskinlæringsmodel, der har potentialet til at gøre søgningen efter energi- og miljømaterialer mere effektiv. Gihan Panapitiya, en dokt -
 Hvad driver kemiske reaktioner? Nøglefaktorer forklaretAf John Brennan Opdateret 30. august 2022 Kemiske reaktioner opstår, når to eller flere stoffer kolliderer og omarrangeres for at danne nye forbindelser. Disse processer er ikke kun allestedsnærvære
Hvad driver kemiske reaktioner? Nøglefaktorer forklaretAf John Brennan Opdateret 30. august 2022 Kemiske reaktioner opstår, når to eller flere stoffer kolliderer og omarrangeres for at danne nye forbindelser. Disse processer er ikke kun allestedsnærvære -
 Mestring af opløselighedsregler:En praktisk vejledning for kemistuderendeAf John Brennan, Opdateret 30. august 2022 Når du starter med kemi, er et solidt greb om opløselighedsreglerne afgørende. I stedet for udenadshukommelse hjælper disse regler dig med at forudsige, hvi
Mestring af opløselighedsregler:En praktisk vejledning for kemistuderendeAf John Brennan, Opdateret 30. august 2022 Når du starter med kemi, er et solidt greb om opløselighedsreglerne afgørende. I stedet for udenadshukommelse hjælper disse regler dig med at forudsige, hvi -
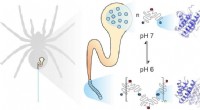 Dynamikken af silkeproteiner er nøglen til enestående stabilitet af edderkoppesilke som biomater…Edderkoppesilke er sammensat af individuelle proteiner. Mekaniske og kemiske faktorer påvirker, hvordan de samles. Underenhedernes dynamik spiller en vigtig rolle. Kredit:Benedikt Goretzki, Ute Hellmi
Dynamikken af silkeproteiner er nøglen til enestående stabilitet af edderkoppesilke som biomater…Edderkoppesilke er sammensat af individuelle proteiner. Mekaniske og kemiske faktorer påvirker, hvordan de samles. Underenhedernes dynamik spiller en vigtig rolle. Kredit:Benedikt Goretzki, Ute Hellmi
- Hvor meget bevæger det menneskelige tyngdepunkt sig lodret, mens de går?
- Hvad er de typer stamceller?
- Bedre end virkeligheden:NASA-forskere bruger virtual reality for at gøre en videnskabelig opdagelse
- En opdagelse af et sort hul kunne tvinge os til at genoverveje, hvordan galakser opstod
- Hvem udfordrede den aristoteliske model af et geocentrisk univers, der begyndte videnskabelig revolu…
- NASA -satellitter ser den tropiske storm Muifa i det nordvestlige Stillehav


