Kobber- og salpetersyrereaktion:Forståelse af kemien
* Kobbers egenskaber: Kobber er et relativt ureaktivt metal, hvilket betyder, at det ikke let giver afkald på sine elektroner. Det kan dog oxideres af stærke oxidationsmidler.
* Salpetersyres egenskaber: Salpetersyre er et stærkt oxidationsmiddel. Den indeholder nitrationen (NO3⁻), som let accepterer elektroner.
* Reaktionen: Når kobber reagerer med salpetersyre, oxiderer nitrationen (NO₃⁻) fra salpetersyre kobberatomerne og trækker elektroner væk fra dem. Dette resulterer i dannelsen af kobberioner (Cu²⁺). Nitrationerne reduceres til nitrogenoxider (NO₂ eller NO) i processen.
Her er en forenklet kemisk ligning:
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
Nøglepunkter:
* Oxidation: Kobber oxideres, mister elektroner og bliver til kobberioner.
* Reduktion: Nitrationer reduceres, får elektroner og bliver til nitrogenoxider.
* Danning af kobbernitrat: Kobberionerne kombineres med nitrationer og danner kobbernitrat (Cu(NO₃)₂), en opløselig forbindelse.
* Rød-brun gas: Den producerede nitrogendioxid (NO2)-gas er en rødbrun farve, som ofte observeres i reaktionen.
Vigtig bemærkning: Reaktionen mellem kobber og salpetersyre producerer ikke hydrogengas (H2), i modsætning til reaktionen af mange metaller med andre syrer som saltsyre. Dette skyldes, at salpetersyre er et stærkt nok oxidationsmiddel til at forhindre dannelsen af brint.
Sidste artikelKobber- og salpetersyrereaktion:En omfattende analyse
Næste artikelKobber- og salpetersyrereaktion:en detaljeret forklaring
 Varme artikler
Varme artikler
-
 Molekylære fabrikker:Kombinationen mellem natur og kemi er funktionelPå molekylære fabrikker injiceret i zebrafiskembryoner, en farvereaktion opstår, når det fangede enzym (peroxidase) virker. Forskerne beviser således, at kombinationen af syntetiske organeller og na
Molekylære fabrikker:Kombinationen mellem natur og kemi er funktionelPå molekylære fabrikker injiceret i zebrafiskembryoner, en farvereaktion opstår, når det fangede enzym (peroxidase) virker. Forskerne beviser således, at kombinationen af syntetiske organeller og na -
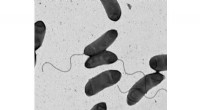 En usædvanlig form for antibiotikaresistens ved pandemisk koleraBilledet er et elektronmikrografi af bakterien Vibrio kolerae , det forårsagende middel til koleraen. Kredit:M. Stephen Trent, University of Georgia Kolera er en ødelæggende sygdom for millioner
En usædvanlig form for antibiotikaresistens ved pandemisk koleraBilledet er et elektronmikrografi af bakterien Vibrio kolerae , det forårsagende middel til koleraen. Kredit:M. Stephen Trent, University of Georgia Kolera er en ødelæggende sygdom for millioner -
 Forskere bruger maskinlæringsteknik til hurtigt at evaluere nye overgangsmetalforbindelserResultater fra en analyse af kunstigt neuralt netværk (ANN) er muligvis ikke pålidelige for molekyler, der er for forskellige fra dem, som ANN blev trænet på. De sorte skyer, der er vist her, dækker o
Forskere bruger maskinlæringsteknik til hurtigt at evaluere nye overgangsmetalforbindelserResultater fra en analyse af kunstigt neuralt netværk (ANN) er muligvis ikke pålidelige for molekyler, der er for forskellige fra dem, som ANN blev trænet på. De sorte skyer, der er vist her, dækker o -
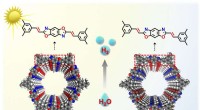 Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab
Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab
- Højesteret kunne tillade sag over salg af Apple iPhone apps
- Hvad er definitionen for geolog?
- Hvilken kraft bekæmper tyngdekraften?
- Sammenlign mængden af arbejde, der er udført, når en kraft 2n bevæger sig et objekt 3 meter me…
- NASA Voyager 2 kan nærme sig det interstellare rum
- 20 millioner år gammel havko med stødtænder er Mellemamerikas ældste havpattedyr


