Valenselektroner:Nøglespillerne i kemiske reaktioner
Her er hvorfor:
* Valenselektroner er elektronerne i et atoms yderste energiniveau. De er dem, der er længst væk fra kernen og oplever den svageste tiltrækning til den. Dette gør dem relativt nemme at vinde, miste eller dele under kemisk binding.
* Indre elektroner (også kaldet kerneelektroner) er tættere på kernen og er tæt bundet. De er typisk ikke involveret i kemiske reaktioner.
Eksempler:
* Ionisk binding: Atomer får eller mister valenselektroner for at danne ioner med fulde ydre skaller, hvilket fører til elektrostatisk tiltrækning.
* Kovalent binding: Atomer deler valenselektroner for at opnå en stabil konfiguration.
Sammenfattende er valenselektroner nøglespillerne i kemiske reaktioner, fordi de bestemmer et atoms reaktivitet, og hvordan det interagerer med andre atomer.
 Varme artikler
Varme artikler
-
 Svovlfjernende bakterier kan være nøglen til at lave fælles komponent i plastikForskere har opdaget, hvordan mikrober i vandlidende jorde producerer høje niveauer af ethylen, hvilket kan have en negativ indvirkning på landbrugsafgrøder og bioenergiråvarer som skiftegræs. Denne n
Svovlfjernende bakterier kan være nøglen til at lave fælles komponent i plastikForskere har opdaget, hvordan mikrober i vandlidende jorde producerer høje niveauer af ethylen, hvilket kan have en negativ indvirkning på landbrugsafgrøder og bioenergiråvarer som skiftegræs. Denne n -
 Selvreplikator, der samtidig skabes og ødelægges, kan føre til en bedre forståelse af livet(Venstre) Koncentration af forskellige forbindelser:råmaterialer (blå), produkt (rød), affaldsprodukt (sort). (Til højre) Selvreplikationsproces. Kredit:Colomer et al. Udgivet i Naturkommunikation .
Selvreplikator, der samtidig skabes og ødelægges, kan føre til en bedre forståelse af livet(Venstre) Koncentration af forskellige forbindelser:råmaterialer (blå), produkt (rød), affaldsprodukt (sort). (Til højre) Selvreplikationsproces. Kredit:Colomer et al. Udgivet i Naturkommunikation . -
 Banebrydende teknik baner vej for hurtig og billig fremstilling af hurtige medicinske diagnostiske v…Eksempel 100-mikron brede 3D-printede mikrokanalstilladser, vist ved siden af en 20p -mønt - omkostningerne ved at udskrive 1000 af disse kanaler. Kredit:University of Bristol Ny teknologi udvik
Banebrydende teknik baner vej for hurtig og billig fremstilling af hurtige medicinske diagnostiske v…Eksempel 100-mikron brede 3D-printede mikrokanalstilladser, vist ved siden af en 20p -mønt - omkostningerne ved at udskrive 1000 af disse kanaler. Kredit:University of Bristol Ny teknologi udvik -
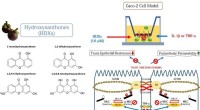 Replikation af mangostan-skalekstrakt som behandling af tarmbetændelse hos mennesker og dyrGrafisk abstrakt. Kredit:Journal of Functional Foods (2021). DOI:10.1016/j.jff.2021.104814 En gruppe forskere i Thailand har replikeret Hydroxy-xanthones, de antioxidantrige livsvigtige ekstrakter,
Replikation af mangostan-skalekstrakt som behandling af tarmbetændelse hos mennesker og dyrGrafisk abstrakt. Kredit:Journal of Functional Foods (2021). DOI:10.1016/j.jff.2021.104814 En gruppe forskere i Thailand har replikeret Hydroxy-xanthones, de antioxidantrige livsvigtige ekstrakter,
- Forklar den måde, hvorpå forskellige seismiske bølger påvirker sten, når de rejser gennem den?
- Vanskeligt terræn:Hjælper med at sikre en sikker roverlanding
- Hvilke klipper er huler lavet af?
- Hvad er 3 klimatyper i Niger River Basin?
- De fire elementer:Udforskning af ild, vand, jord og luft - hvad er stærkest?
- Ny undersøgelse afslører lavere energigrænse for liv på Jorden


