Hydrogenbinding:Elementer og bindingsdannelse
* Mere elektronegativ end brint: Dette omfatter elementer som oxygen, nitrogen, fluor, klor og brom. Elektronegativitetsforskellen mellem hydrogen og disse grundstoffer fører til dannelsen af polære kovalente bindinger , hvor elektronerne deles ulige, hvilket resulterer i delvise positive og negative ladninger på atomerne. Dette er en væsentlig drivkraft bag hydrogenbinding.
* Lille og meget elektronegativ: Dette er grunden til, at brint let danner bindinger med oxygen og nitrogen, men ikke med tungere grundstoffer som svovl eller fosfor, selvom de er elektronegative.
Her er en opdeling af de typer bindinger, hydrogen danner med forskellige grundstoffer:
1. Kovalente bindinger:
* Polære kovalente bindinger: Disse bindinger dannes med stærkt elektronegative elementer som oxygen, nitrogen, fluor, klor og brom. Den ulige deling af elektroner fører til partielle ladninger, hvilket gør hydrogenbinding mulig.
* Eksempler:Vand (H₂O), ammoniak (NH₃), methan (CH₄)
* Ikke-polære kovalente bindinger: Disse bindinger dannes med elementer som kulstof og silicium, hvor elektronegativitetsforskellen er minimal.
* Eksempler:Metan (CH₄), silan (SiH₄)
2. Hydrogenbindinger:
* Hydrogenbindinger er en særlig type interaktion mellem et brintatom, der er kovalent bundet til et stærkt elektronegativt atom (som oxygen, nitrogen eller fluor) og et elektronpar på et tilstødende molekyle. Denne interaktion er stærkere end en typisk dipol-dipol-interaktion, men svagere end en kovalent binding.
* Eksempler:Vand (H₂O), DNA, proteiner
3. Ioniske bindinger:
* Brint kan danne ioniske bindinger med stærkt elektronegative elementer som fluor, klor og brom, men disse er mindre almindelige.
* Eksempler:Hydrogenfluorid (HF)
Sammenfattende kan brint danne en række bindinger afhængigt af elektronegativiteten og størrelsen af det andet involverede element. Dens evne til at danne hydrogenbindinger med stærkt elektronegative elementer er afgørende for strukturen og egenskaberne af mange vigtige molekyler inden for biologi og kemi.
 Varme artikler
Varme artikler
-
 Polære vs. ikke-polære bindinger:Hvordan elektronegativitet former kemiske egenskaberAf Riti GuptaOpdateret 30. august 2022 JK1991/iStock/GettyImages Elektronegativitet er den drivkraft, der bestemmer, hvor stærkt et atom tiltrækker elektroner. Jo større et atoms elektronegativitet,
Polære vs. ikke-polære bindinger:Hvordan elektronegativitet former kemiske egenskaberAf Riti GuptaOpdateret 30. august 2022 JK1991/iStock/GettyImages Elektronegativitet er den drivkraft, der bestemmer, hvor stærkt et atom tiltrækker elektroner. Jo større et atoms elektronegativitet, -
 Solbrint:Lad os overveje stabiliteten af fotoelektroderSkalerbart stort område BiVO 4 fotoanode på FTO med Ni strømaftagere. Kredit:HZB Brint er et alsidigt brændstof, der kan lagre og frigive kemisk energi, når det er nødvendigt. Brint kan producer
Solbrint:Lad os overveje stabiliteten af fotoelektroderSkalerbart stort område BiVO 4 fotoanode på FTO med Ni strømaftagere. Kredit:HZB Brint er et alsidigt brændstof, der kan lagre og frigive kemisk energi, når det er nødvendigt. Brint kan producer -
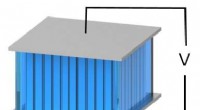 Træbaseret teknologi skaber elektricitet fra varmeKredit:University of Maryland Et team af forskere, der ledes af University of Maryland, har skabt en varme-til-elektricitetsenhed, der kører på ioner, og som en dag kan udnytte kroppens varme for
Træbaseret teknologi skaber elektricitet fra varmeKredit:University of Maryland Et team af forskere, der ledes af University of Maryland, har skabt en varme-til-elektricitetsenhed, der kører på ioner, og som en dag kan udnytte kroppens varme for -
 Syntese af bio-baseret højtydende polyamid fra biogene resterEt forskerhold fra Fraunhofer Institute for Interfacial Engineering and Biotechnology (IGB) og Münchens tekniske universitet (TUM) ledet af kemiker Volker Sieber har udviklet en ny polyamidfamilie, de
Syntese af bio-baseret højtydende polyamid fra biogene resterEt forskerhold fra Fraunhofer Institute for Interfacial Engineering and Biotechnology (IGB) og Münchens tekniske universitet (TUM) ledet af kemiker Volker Sieber har udviklet en ny polyamidfamilie, de
- Strømsvigt:Hvordan en vinterstorm skubbede Texas i krise
- Mikrober fester på knust klippe i subglaciale søer under Antarktis
- Hvad er de egenskaber egenskaber på jorden, der gør livet muligt, som vi kender det?
- Hvordan skriver du enhederne til vægt, når Multiply Mass Times kraft på grund af acceleration af …
- Hvordan bærer dine kroppe elektricitet?
- Knight of Wands Tarotkort:Slip din indre ild løs


