Forståelse af oxidationstal:Hvorfor rene elementer har 0
* Det findes i sin elementære form: Det betyder, at grundstoffet ikke er bundet til andre atomer. Der er ingen deling eller overførsel af elektroner i selve elementet.
* Ingen nettoafgift: Da der ikke er nogen binding, er der ingen forskel i elektronegativitet mellem atomer af samme grundstof. Dette betyder, at der ikke er nogen gevinst eller tab af elektroner, hvilket resulterer i en neutral ladning.
* Oxidationsnumre tildeles baseret på elektrondeling: Oxidationstal repræsenterer den hypotetiske ladning et atom ville have, hvis alle bindingerne var rent ioniske (komplet overførsel af elektroner). I et rent grundstof er der ingen elektronoverførsel, så oxidationstallet er tildelt 0.
Her er nogle eksempler:
* Oxygen (O2): Hvert oxygenatom har et oxidationstal på 0 i det diatomiske oxygenmolekyle.
* Natrium (Na): Et enkelt natriumatom har et oxidationstal på 0.
* Kobber (Cu): Et stykke rent kobbermetal har et oxidationstal på 0 for alle kobberatomerne.
Opsummering: Oxidationstallet for et rent grundstof er 0, fordi det ikke er bundet til andre atomer, og der er ingen nettoladning på grund af fraværet af elektronoverførsel.
Sidste artikelHydrogenbinding:Elementer og bindingsdannelse
Næste artikelIoniske forbindelser dannet af natrium:reagerer med to atomer
 Varme artikler
Varme artikler
-
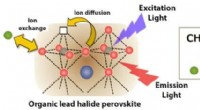 Succes med at kontrollere sammensætningen af perovskitioner baner vejen for enhedsapplikationerIonadfærd i organisk blyhalogenidperovskit. Bromidionen (Br-) i opløsningen kan let udskiftes med iodidionen (I-) inde i krystallen. Bevægelsen af halogenidionerne inde i krystallen foranlediges af
Succes med at kontrollere sammensætningen af perovskitioner baner vejen for enhedsapplikationerIonadfærd i organisk blyhalogenidperovskit. Bromidionen (Br-) i opløsningen kan let udskiftes med iodidionen (I-) inde i krystallen. Bevægelsen af halogenidionerne inde i krystallen foranlediges af -
 Ny 3D-printproces tilbyder nye muligheder for energilagringsdesignForskere ved UNSW Sydney brugte en standard 3D-printer til at producere et indviklet kort over Australien lavet af fast polymerelektrolyt, som derefter blev testet som en energilagringsenhed. Kredit:D
Ny 3D-printproces tilbyder nye muligheder for energilagringsdesignForskere ved UNSW Sydney brugte en standard 3D-printer til at producere et indviklet kort over Australien lavet af fast polymerelektrolyt, som derefter blev testet som en energilagringsenhed. Kredit:D -
 Virkningen af stigningen i afvisning af nye lægemidlerKredit:CC0 Public Domain Antallet af nye lægemiddelansøgninger afvist af U.S. Food and Drug Administration har været stigende. Forsidehistorien om Nyheder om kemi og teknik ( C&EN ), det ugent
Virkningen af stigningen i afvisning af nye lægemidlerKredit:CC0 Public Domain Antallet af nye lægemiddelansøgninger afvist af U.S. Food and Drug Administration har været stigende. Forsidehistorien om Nyheder om kemi og teknik ( C&EN ), det ugent -
 Knap ridser overfladen:En ny måde at lave robuste membraner påEn ny Argonne-teknik kan dyrke materiale inde i membranstrukturer, ændre deres kemi uden at påvirke poreformen markant. Dette giver forskere mulighed for at forbedre membraner på forskellige måder. Kr
Knap ridser overfladen:En ny måde at lave robuste membraner påEn ny Argonne-teknik kan dyrke materiale inde i membranstrukturer, ændre deres kemi uden at påvirke poreformen markant. Dette giver forskere mulighed for at forbedre membraner på forskellige måder. Kr
- Det gentagne mønster af et mineral og partikler danner fast kaldet A (N)?
- Hvor kan jeg købe stjernekiggerbriller af høj kvalitet til en mindeværdig himmelsk seoplevelse?
- Afbrænding af afgrøderester er en væsentlig bidragyder til luftforurening i Sydasien
- Hvorfor kaldes areal en afledt størrelse?
- Mysterium om sjældne vulkaner på Venus
- Hvad er universel energi?


