Oxygenbinding:Forståelse af ilts kemiske egenskaber
Her er hvorfor:
* Oxygen har seks valenselektroner. Valenselektroner er de yderste elektroner, der er involveret i binding.
* Oxygen har brug for to elektroner mere for at fuldføre sin oktet. En oktet er en stabil konfiguration med otte elektroner i sin ydre skal.
* Oxygen opnår dette ved at danne to kovalente bindinger. Kovalente bindinger involverer deling af elektroner mellem atomer.
Lad mig vide, hvis du gerne vil vide mere om kovalent binding eller andre aspekter af oxygens kemi!
Sidste artikelUdvidet strukturformel for propan:En klar forklaring
Næste artikelFerrocyanidformel:Forståelse af [Fe(CN)₆]⁴⁻
 Varme artikler
Varme artikler
-
 Går småt for at bestemme, hvor nukleart materiale kom fra, og hvordan det blev lavetIn-situ uran-isotop-billeddannelse af NanoSIMS kan give indsigt i proceshistorien og oprindelsen af materialer til nukleare brændstofpellets til støtte for nuklear retsmedicinske undersøgelser. Kred
Går småt for at bestemme, hvor nukleart materiale kom fra, og hvordan det blev lavetIn-situ uran-isotop-billeddannelse af NanoSIMS kan give indsigt i proceshistorien og oprindelsen af materialer til nukleare brændstofpellets til støtte for nuklear retsmedicinske undersøgelser. Kred -
 Ny bæredygtig produktionsmetode kan fremme plast og lægemidlerIngeniører fra University of Texas viser deres skoleånd frem ved at støbe den nye, bæredygtigt produceret plastmateriale til en Longhorn-silhuet i Hal Alpers laboratorium. Kredit:Cockrell School of En
Ny bæredygtig produktionsmetode kan fremme plast og lægemidlerIngeniører fra University of Texas viser deres skoleånd frem ved at støbe den nye, bæredygtigt produceret plastmateriale til en Longhorn-silhuet i Hal Alpers laboratorium. Kredit:Cockrell School of En -
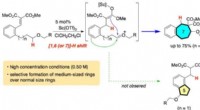 Forskere udvikler metode til at forbedre skelettet af almindelige kemikalierForskere i Japan udviklede en ny metode til at producere mere komplicerede og mellemstore (syv- og otte-leddede) carbocycles. Kredit:Keiji Mori, TUAT Ethvert kemikalie, fra det enkleste til det me
Forskere udvikler metode til at forbedre skelettet af almindelige kemikalierForskere i Japan udviklede en ny metode til at producere mere komplicerede og mellemstore (syv- og otte-leddede) carbocycles. Kredit:Keiji Mori, TUAT Ethvert kemikalie, fra det enkleste til det me -
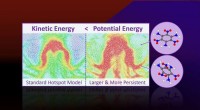 Forskning afdækker manglende fysik i eksplosive hotspotsMolekylær dynamik simuleringer forudsiger, at mere potentiel energi er lokaliseret i hotspots, end deres kinetiske energi (eller temperatur) antyder. Overskydende potentiel energi er bundet til vedvar
Forskning afdækker manglende fysik i eksplosive hotspotsMolekylær dynamik simuleringer forudsiger, at mere potentiel energi er lokaliseret i hotspots, end deres kinetiske energi (eller temperatur) antyder. Overskydende potentiel energi er bundet til vedvar
- Hvad er de vigtigste komponenter i planetarisk kredsløbsmodel, og hvordan forklarer de bevægelsesc…
- Hvordan får statisk elektricitet til at bevæge sig?
- Hvorfor ændres højden på Eiffeltårnet med 7,5 cm mellem sommeren?
- Hvad hedder de små pakker med energi, der skaber lys?
- Ny undersøgelse afslører øget snefald i Antarktis i løbet af de sidste to århundreder
- Hvor lang tid tager det at få månen i Odyssey?


