Periodisk system:Gruppeplacering af grundstof 115
Her er hvorfor:
* Gruppenummer og valenselektroner: Gruppenumre i det periodiske system svarer generelt til antallet af valenselektroner (elektroner i den yderste skal) et grundstof har.
* Elektronkonfiguration: Grundstoffer i gruppe 15 har alle 5 valenselektroner i deres yderste skal. Dette bestemmes af deres elektronkonfiguration, som for grundstoffer i gruppe 15 ender på ns²np³.
* Element 115: Grundstof 115 (Moscovium) har elektronkonfigurationen [Rn] 5f¹⁴ 6d¹⁰ 7s² 7p³. Den har 5 valenselektroner (7s² 7p³), hvilket placerer den i gruppe 15.
Derfor ville et syntetisk grundstof med 115 protoner være medlem af gruppe 15.
Sidste artikelThoriumoxider:egenskaber, formler og farer
Næste artikelBestem den empiriske formel for et oxid fra rød fosforforbrænding
 Varme artikler
Varme artikler
-
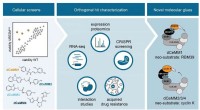 Lægemiddelopdagelse:Første rationelle strategi for at finde molekylære limnedbrydereCellular levedygtighedsskærme nominerede potentielle molekylære lim. Ortogonal undersøgelse af de førende molekyler (dCeMM1/2/3/4) muliggjorde karakterisering af nye molekylære limnedbrydere, der rekr
Lægemiddelopdagelse:Første rationelle strategi for at finde molekylære limnedbrydereCellular levedygtighedsskærme nominerede potentielle molekylære lim. Ortogonal undersøgelse af de førende molekyler (dCeMM1/2/3/4) muliggjorde karakterisering af nye molekylære limnedbrydere, der rekr -
 Hvordan pH-ændringer påvirker biologiske systemerAf Jacob Stutsman, Opdateret 30. august 2022 pH-skalaen kvantificerer en opløsnings surhedsgrad ved at måle dens hydrogenionkoncentration. Biologiske systemer afhænger af et snævert pH-område; selv b
Hvordan pH-ændringer påvirker biologiske systemerAf Jacob Stutsman, Opdateret 30. august 2022 pH-skalaen kvantificerer en opløsnings surhedsgrad ved at måle dens hydrogenionkoncentration. Biologiske systemer afhænger af et snævert pH-område; selv b -
 Nøglegasser, der driver ozonnedbrydning:Årsager og virkningJupiterimages/Comstock/Getty Images I den øvre del af Jordens stratosfære absorberer et tyndt lag af ozonmolekyler ultraviolet sollys, hvilket gør forholdene ved overfladen befordrende for levende væ
Nøglegasser, der driver ozonnedbrydning:Årsager og virkningJupiterimages/Comstock/Getty Images I den øvre del af Jordens stratosfære absorberer et tyndt lag af ozonmolekyler ultraviolet sollys, hvilket gør forholdene ved overfladen befordrende for levende væ -
 Raman-spektroskopi giver ikke-invasiv måde at spore celleprogrammering påFigur 1:Raman -spektroskopi bruger laserlys til at karakterisere den kemiske sammensætning af prøver. RIKEN -forskere har nu brugt Raman -spektroskopi til at spore de kemiske ændringer, der sker, når
Raman-spektroskopi giver ikke-invasiv måde at spore celleprogrammering påFigur 1:Raman -spektroskopi bruger laserlys til at karakterisere den kemiske sammensætning af prøver. RIKEN -forskere har nu brugt Raman -spektroskopi til at spore de kemiske ændringer, der sker, når
- Hvilken form bruger mennesker kulhydrater?
- En ny ordning for satellitbaseret kvantesikker tidsoverførsel
- Facebooks kryptovaluta står over for en præ-G20-undersøgelse
- Hvordan påvirker en ændring i temperatur fra 25o til 50o reaktionshastigheden?
- Hvad er den eksterne del af STEM og deres funktion?
- De første blomster udviklede sig før bier – så hvordan blev de så blændende?


