Væsker vs. gasser:Forståelse af molekylær struktur og egenskaber
Her er en oversigt:
* Væsker: Molekylerne i en væske er tæt på hinanden, men kan bevæge sig rundt om hinanden. De har et fast volumen, men ikke en fast form.
* Gasser: Molekylerne i en gas er langt fra hinanden og bevæger sig frit i alle retninger. De har ingen fast volumen eller form.
Nøgleforskelle:
* Mellemrum: Molekyler i væsker er tættere på hinanden end i gasser.
* Bevægelse: Molekyler i væsker bevæger sig mere frit end i faste stoffer, men mindre frit end i gasser.
* Form: Væsker tager form af deres beholder, mens gasser fylder hele beholderen, de er i.
Eksempel:
* Vand (flydende): Vandmolekyler er tæt på hinanden, men kan bevæge sig rundt, så det kan flyde.
* Luft (gas): Luftmolekyler er langt fra hinanden og bevæger sig frit, hvilket gør luft komprimerbar.
Vigtig bemærkning: Mens vi ofte taler om, at væsker og gasser består af molekyler, er der nogle stoffer (som elementære metaller som kviksølv), der eksisterer som væsker ved stuetemperatur, selvom deres struktur ikke er baseret på individuelle molekyler.
Sidste artikelForståelse af Brønsted-Lowry Bases:Definition &Eksempler
Næste artikelForstå væsker:sammensætning, egenskaber og typer
 Varme artikler
Varme artikler
-
 Partikler fra dagligdags vægmaling kan skade levende organismer, men en ny membran viser høje filt…Kredit:Ann-Kathrin Müller et al., Økotoksikologi og miljøsikkerhed (2022). DOI:10.1016/j.ecoenv.2022.113877 Dispersionsmalinger bruges mest i husholdninger til maling af vægge og lofter. Et tværfag
Partikler fra dagligdags vægmaling kan skade levende organismer, men en ny membran viser høje filt…Kredit:Ann-Kathrin Müller et al., Økotoksikologi og miljøsikkerhed (2022). DOI:10.1016/j.ecoenv.2022.113877 Dispersionsmalinger bruges mest i husholdninger til maling af vægge og lofter. Et tværfag -
 Laboratoriepræparation af oxalsyre fra sukker og salpetersyreAf Allan Robinson, opdateret 30. august 2022 Oxalsyre (H₂C₂O4) er en moderat organisk syre, der ofte tjener som et reduktionsmiddel i organisk syntese. Det kan syntetiseres i et laboratorium ved hjæl
Laboratoriepræparation af oxalsyre fra sukker og salpetersyreAf Allan Robinson, opdateret 30. august 2022 Oxalsyre (H₂C₂O4) er en moderat organisk syre, der ofte tjener som et reduktionsmiddel i organisk syntese. Det kan syntetiseres i et laboratorium ved hjæl -
 Ny kernemagnetisk resonansspektroskopi-forskning afslører dynamikken af katalysatorer i 3D-rumKredit: Uorganisk kemi grænser (2020). DOI:10.1039/D0QI01241F Forskere fra det amerikanske energiministeriums Ames Laboratory har kortlagt dynamikken i en katalysators aktive sted i tre dimension
Ny kernemagnetisk resonansspektroskopi-forskning afslører dynamikken af katalysatorer i 3D-rumKredit: Uorganisk kemi grænser (2020). DOI:10.1039/D0QI01241F Forskere fra det amerikanske energiministeriums Ames Laboratory har kortlagt dynamikken i en katalysators aktive sted i tre dimension -
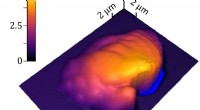 Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord
Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord
- Hvad er kvantiserede energiniveau?
- Afsløret manglende trin i lipiddannelsen kunne muliggøre påvisning af tidligere klimaer
- En bil kører med en konstant hastighed på cirkulær spor af radius 200 meter, der tager 62,8 sekun…
- En ny måde at vurdere mandlig fertilitet på
- Et æble falder på grund af tyngdekraften til Jorden. Hvordan sammenligner Jorden?
- Nøglefaktorer, der orkestrerer mystisk synkroniseret koral-gydning, afsløret


