Forståelse af Brønsted-Lowry Bases:Definition &Eksempler
Brønsted-Lowry-teori:
* Fokuserer på overførsel af protoner (H+) under syre-base reaktioner.
* Syre: Et stof, der donerer en proton (H+).
* Basis: Et stof, der accepterer en proton (H+).
Hvordan et stof fungerer som en Brønsted-Lowry base:
1. Tilstedeværelse af et ensomt par: Brønsted-Lowry baser har typisk et ensomt elektronpar. Dette enlige par er tilgængeligt til at danne en binding med en proton (H+).
2. Reaktion med en syre: Når en Brønsted-Lowry-base reagerer med en syre, accepterer den en proton fra syren. Dette danner en ny binding mellem basen og protonen.
Eksempel:
* Ammoniak (NH3) er en Brønsted-Lowry base. Det har et ensomt elektronpar på nitrogenatomet.
* Vand (H2O) kan fungere som både en Brønsted-Lowry syre og base.
* Som en syre: Det kan donere en proton (H+), der danner hydroxidionen (OH-).
* Som base: Det kan acceptere en proton (H+), der danner hydroniumionen (H3O+).
Nøglepunkter at huske:
* Brønsted-Lowry baser er ikke nødvendigvis hydroxidholdige forbindelser.
* De kan være molekyler, ioner eller endda atomer.
* Et stofs evne til at fungere som base afhænger af dets specifikke kemiske struktur og reaktionsbetingelserne.
 Varme artikler
Varme artikler
-
 Meget effektiv metode til syntetisering af polyisoprengummi med ultrahøj molekylvægtKredit:Unsplash/CC0 Public Domain Forgrenede polydiengummier med ultrahøj molekylvægt besidder bemærkelsesværdige mekaniske egenskaber, såsom høj trækstyrke, høj vådskridningsmodstand, og høj dæmp
Meget effektiv metode til syntetisering af polyisoprengummi med ultrahøj molekylvægtKredit:Unsplash/CC0 Public Domain Forgrenede polydiengummier med ultrahøj molekylvægt besidder bemærkelsesværdige mekaniske egenskaber, såsom høj trækstyrke, høj vådskridningsmodstand, og høj dæmp -
 Nye algoritmer vist at accelerere biofarmaceutisk procesKredit:Rensselaer Polytekniske Institut Biofarmaceutiske midler er nødvendige, livreddende værktøjer. Men processen for at lave dem er tidskrævende og dyr, især når det kommer til rensningsprocess
Nye algoritmer vist at accelerere biofarmaceutisk procesKredit:Rensselaer Polytekniske Institut Biofarmaceutiske midler er nødvendige, livreddende værktøjer. Men processen for at lave dem er tidskrævende og dyr, især når det kommer til rensningsprocess -
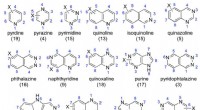 Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114
Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114 -
 Varmebehandling giver præcis kontrol over katalytisk aktivitet af metalsulfidnanopartiklerDette scanningselektronmikroskopbillede (forstørrelse x100, 000) viser overfladen af et porøst nikkelskum, der er krydret med katalytiske nanopartikler af koboltsulfid og nikkelsulfid. Kredit:A*STAR
Varmebehandling giver præcis kontrol over katalytisk aktivitet af metalsulfidnanopartiklerDette scanningselektronmikroskopbillede (forstørrelse x100, 000) viser overfladen af et porøst nikkelskum, der er krydret med katalytiske nanopartikler af koboltsulfid og nikkelsulfid. Kredit:A*STAR
- Hvad gør delene af hjernen kontrol?
- Chimpanser i naturen ændrer advarsler baseret på, hvad andre, deres gruppe allerede ved, viser und…
- Hvilket astronomisk instrument måler stjernens lysstyrke?
- Hvad sker der med en prøve af stof, når dens partikler mister kinetisk energi?
- Hvad vi ved om orkanen Irma:fakta, tal, Vejrudsigt
- Hvordan understøtter forskellige miljøer varianter af organismer?


