Kovalente bindinger:Forståelse af elektrondeling i kemi
Her er en oversigt:
* Kovalente bindinger opstår, når to eller flere atomer deler elektroner i deres yderste skal (valensskaller). Denne deling gør det muligt for atomerne at opnå en stabil elektronkonfiguration, der ligner ædelgasser.
* De delte elektroner tiltrækkes af kernerne i begge atomer og holder dem sammen.
* Kovalente bindinger kan være enkelt-, dobbelt- eller tredobbelt , afhængigt af antallet af elektronpar, der deles.
Her er nogle nøgletræk ved kovalente bindinger:
* Stærke bånd: Kovalente bindinger er generelt stærkere end andre typer bindinger, såsom ionbindinger.
* Retningsbestemt: Kovalente bindinger har en specifik retningsbestemthed, hvilket betyder, at de delte elektroner er placeret mellem de to kerner. Dette giver molekyler en bestemt form.
* Ikke-polær og polær: Kovalente bindinger kan være ikke-polære (lige deling af elektroner) eller polære (ulige deling af elektroner).
Eksempler på molekyler dannet af kovalente bindinger:
* Vand (H2O) :Hvert brintatom deler en elektron med oxygenatomet og danner to enkelt kovalente bindinger.
* Culdioxid (CO2) :Kulstofatomet deler to elektroner med hvert oxygenatom og danner to dobbeltkovalente bindinger.
* Metan (CH4) :Kulstofatomet deler én elektron med hver af de fire brintatomer og danner fire enkelt kovalente bindinger.
Fortæl mig, hvis du gerne vil vide mere om specifikke typer kovalente bindinger eller egenskaberne af molekyler dannet af dem.
Sidste artikelBrom- og vandreaktion:Disproportionering forklaret
Næste artikelTetrabrommethanbindinger:Forståelse af kovalent binding i CBr₄
 Varme artikler
Varme artikler
-
 Hvorfor det er vigtigt at kalibrere dit pH-måler og elektroder med standardbuffereAf Philip J. Carlson, Opdateret 24. marts 2022 Grundlæggende om et pH-meter Et pH-meter måler potentialforskellen skabt af en glaselektrode, der selektivt tillader hydrogenioner (H⁺) at passere igenn
Hvorfor det er vigtigt at kalibrere dit pH-måler og elektroder med standardbuffereAf Philip J. Carlson, Opdateret 24. marts 2022 Grundlæggende om et pH-meter Et pH-meter måler potentialforskellen skabt af en glaselektrode, der selektivt tillader hydrogenioner (H⁺) at passere igenn -
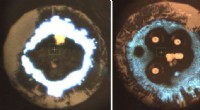 Forskere syntetiserer nyt nitrid og stabiliserer dets hexazinringe ved højt trykMikrofotografier af laseropvarmede kaliumazidprøver ved tryk på 500.000 atmosfærer (venstre) og 300.000 atmosfærer (højre). De hvide til lyseblå områder på ydersiden er K1N3. Mod midten er materialet
Forskere syntetiserer nyt nitrid og stabiliserer dets hexazinringe ved højt trykMikrofotografier af laseropvarmede kaliumazidprøver ved tryk på 500.000 atmosfærer (venstre) og 300.000 atmosfærer (højre). De hvide til lyseblå områder på ydersiden er K1N3. Mod midten er materialet -
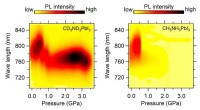 Jo tungere, jo bedre - overlegen stabilitet i isotopfunktionaliserede perovskitterFarveplot af de trykafhængige PL-udviklinger af CD3ND3PbI3 (venstre) og CH3NH3PbI3 (højre) enkeltkrystaller. Kredit:Gang Liu Organisk-uorganisk hybrid blyiodidperovskiter er universelt anerkendt s
Jo tungere, jo bedre - overlegen stabilitet i isotopfunktionaliserede perovskitterFarveplot af de trykafhængige PL-udviklinger af CD3ND3PbI3 (venstre) og CH3NH3PbI3 (højre) enkeltkrystaller. Kredit:Gang Liu Organisk-uorganisk hybrid blyiodidperovskiter er universelt anerkendt s -
 Kulstoffangstprocessen producerer brint og byggematerialerKredit:CC0 Public Domain Ph.D. forsker Olawale Oloye og professor Anthony OMullane fra QUT Center for Clean Energy Technologies and Practices udviklede den elektrokemiske opsamling og omdannelse a
Kulstoffangstprocessen producerer brint og byggematerialerKredit:CC0 Public Domain Ph.D. forsker Olawale Oloye og professor Anthony OMullane fra QUT Center for Clean Energy Technologies and Practices udviklede den elektrokemiske opsamling og omdannelse a
- Spar penge:Bruger forbrugerne mindre, hvis de tænker på fremtiden?
- Lithium-ion anode bruger selvsamlede nanokompositmaterialer for at øge kapaciteten
- Hvad er de ældste levende træer på jorden?
- Hvilken type energi er en fan?
- Undersøgelse viser, at turistindustrien betaler de laveste lønninger i hele landet
- Hvilke kirtler kontrollerer handlingerne fra flere andre kirtler?


