Brom- og vandreaktion:Disproportionering forklaret
Br₂ (l) + H₂O (l) ⇌ HBr (aq) + HOBr (aq)
Her er en oversigt over, hvad der sker:
* Oxidation: Et bromatom får en elektron til at danne bromidion (Br-) i HBr. Dette er en reduktion.
* Reduktion: Det andet bromatom mister en elektron for at danne hypobromition (OBr-) i HOBr. Dette er en oxidation.
Vigtige punkter:
* Reaktionen er reversibel, hvilket betyder, at ligevægten kan skifte afhængigt af forholdene.
* HOBr er en svag syre og et kraftigt oxidationsmiddel. Det er ansvarligt for de blegende og desinficerende egenskaber af bromvand.
* Reaktionen begunstiges af tilstedeværelsen af overskydende vand.
* Farven på bromvand skifter fra orange-brun til bleggul på grund af dannelsen af HOBr.
Applikationer:
Denne reaktion er vigtig i forskellige applikationer, herunder:
* Desinfektion: Bromvand bruges som desinfektionsmiddel i pools og spabade.
* Blegning: HOBr er et kraftigt blegemiddel.
* Organisk syntese: HOBr bruges som reagens i forskellige organiske reaktioner.
Overordnet set er reaktionen mellem brom og vand en kompleks, men vigtig proces, der fører til dannelsen af flere værdifulde kemiske arter.
 Varme artikler
Varme artikler
-
 Omdanner kuldioxid til metan eller etan selektivt(a) Prøvebilleder opnået på forskellige stadier af syntese (b) Kumulativ metan- og etanudvikling for forskellige Pt vægtprocent sensibiliserede 0,50-G/RBT-prøver. Kredit:Daegu Gyeongbuk Institute of S
Omdanner kuldioxid til metan eller etan selektivt(a) Prøvebilleder opnået på forskellige stadier af syntese (b) Kumulativ metan- og etanudvikling for forskellige Pt vægtprocent sensibiliserede 0,50-G/RBT-prøver. Kredit:Daegu Gyeongbuk Institute of S -
 Nye selvsamlende proteinhydrogeler kan rumme mange anvendelser til biomedicinEt omvendt reagensglas rummer det nye bløde proteinhydrogel, der stammer fra naturen. De lægemiddelbindende områder er i rødt, og den stimuli-responsive del er vist i sort; det kan bruges til en række
Nye selvsamlende proteinhydrogeler kan rumme mange anvendelser til biomedicinEt omvendt reagensglas rummer det nye bløde proteinhydrogel, der stammer fra naturen. De lægemiddelbindende områder er i rødt, og den stimuli-responsive del er vist i sort; det kan bruges til en række -
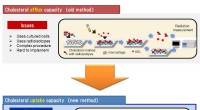 En ny praktisk test for funktionen af HDL, bæreren af det gode kolesterolKolesteroludstrømningskapacitet og optagelseskapacitet er vist. Kredit:Kobe University High-density lipoprotein kolesterol (HDL-C) er kendt som godt kolesterol, fordi HDL-partikler fjerner oversky
En ny praktisk test for funktionen af HDL, bæreren af det gode kolesterolKolesteroludstrømningskapacitet og optagelseskapacitet er vist. Kredit:Kobe University High-density lipoprotein kolesterol (HDL-C) er kendt som godt kolesterol, fordi HDL-partikler fjerner oversky -
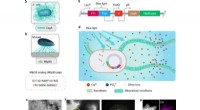 Lysfølsomme E. coli-funktionelle biofilm som stilladser til hydroxyapatitmineraliseringEngineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. Engineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. (a) Skem
Lysfølsomme E. coli-funktionelle biofilm som stilladser til hydroxyapatitmineraliseringEngineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. Engineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. (a) Skem
- Hvad er et navn på den kraft, der gør det svært for stoffet at begynde at bevæge sig?
- Hvad er den potentielle elektriske energi fra et ladet objekt?
- Race og køn stadig et problem på akademiske konferencer
- Gulerodscement:Hvordan rodfrugter og aske kunne gøre beton mere bæredygtig
- Indonesien udvider farezonen omkring ø-vulkanen
- Hvor meget momentum vil en håndvægt af masse 10 kg overføre til gulvet, hvis det falder fra højd…


