Elektronkonfigurationsprincipper:Aufbau og Hunds regel forklaret
1. Aufbau-princippet:
* Dette princip siger, at elektroner fylder orbitaler i rækkefølge efter stigende energi. Det betyder, at vi starter med orbitaler med lavest energi og bevæger os op.
* Energiniveauer bestemmes af det primære kvantetal (n), og underniveauer bestemmes af det azimutale kvantetal (l).
* Rækkefølgen er:1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
2. Hunds regel:
* Denne regel siger, at inden for en subshell (som 2p subshell), vil elektroner individuelt indtage hver orbital inden for den subshell, før de fordobles i en hvilken som helst orbital.
* Det skyldes, at elektroner frastøder hinanden, og de er mest stabile, når de er så langt fra hinanden som muligt.
* Elektroner i forskellige orbitaler inden for den samme underskal har parallelle spins (alle spin op eller alle spin ned).
3. Pauli udelukkelsesprincip:
* Dette princip siger, at ikke to elektroner i et atom kan have det samme sæt af fire kvantetal.
* Det betyder, at hver orbital maksimalt kan rumme to elektroner, og disse to elektroner skal have modsatte spin.
4. "n + l"-reglen (til bestilling af orbitaler):
* Denne regel er en nyttig måde at huske rækkefølgen af udfyldning af orbitaler, især for større atomer.
* Reglen siger, at orbitalen med den laveste værdi af (n + l) udfyldes først. Hvis to orbitaler har samme (n + l) værdi, udfyldes orbitalen med den laveste værdi af n først.
Visuel hjælp:Den diagonale regel
* Du kan visualisere udfyldningsrækkefølgen af orbitaler med diagonalreglen . Dette er et praktisk diagram, der hjælper dig med at huske rækkefølgen af orbitaler baseret på deres energiniveauer.
Eksempel:
Lad os tage grundstoffet Nitrogen (N), som har 7 elektroner.
1. Aufbau-princippet: Start med det laveste energiniveau, 1s. Fyld den med 2 elektroner (1s²).
2. Aufbau-princippet: Flyt til det næstlaveste energiniveau, 2s. Fyld den med 2 elektroner (2s²).
3. Aufbau-princippet og Hunds regel: Flyt til 2p subshell. Dette har 3 orbitaler (2px, 2py, 2pz). Placer en elektron i hver af disse orbitaler med parallelle spin, før du fordobler (2p³, 2p³, 2p³).
Derfor er elektronkonfigurationen af nitrogen 1s² 2s² 2p³.
Vigtige ting:
* Forståelse af disse principper giver dig mulighed for at forudsige elektronkonfigurationen af ethvert atom.
* Elektronkonfiguration er afgørende for at forstå grundstoffernes kemiske adfærd og egenskaber.
* Det hjælper os med at forklare binding, reaktivitet og grundstoffernes periodiske tendenser.
Sidste artikelFuran-reaktivitet:Forståelse af forskelle med pyrrol og thiophen
Næste artikelBrintoxidationstal:Forståelse af +1 og -1
 Varme artikler
Varme artikler
-
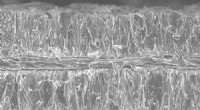 Galvanisering giver høj energi, højeffekts batterierEt elektronmikrografi-tværsnit viser aluminiumsfolie belagt med lithium-koboltoxid, et almindeligt materiale i lithium-ion-batterier. Kredit:Billede udlånt af Hailong Ning og Jerome Davis III, Xerion
Galvanisering giver høj energi, højeffekts batterierEt elektronmikrografi-tværsnit viser aluminiumsfolie belagt med lithium-koboltoxid, et almindeligt materiale i lithium-ion-batterier. Kredit:Billede udlånt af Hailong Ning og Jerome Davis III, Xerion -
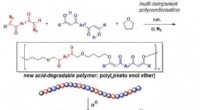 Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde
Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde -
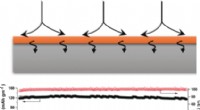 Hybride indium-lithium anoder giver hurtig grænsefladeiontransportNye lithiumelektroder belagt med indium kunne være grundlaget for mere kraftfulde, længerevarende, genopladelige batterier. Belægningen forhindrer uønskede side-reaktioner mellem elektroden og elektro
Hybride indium-lithium anoder giver hurtig grænsefladeiontransportNye lithiumelektroder belagt med indium kunne være grundlaget for mere kraftfulde, længerevarende, genopladelige batterier. Belægningen forhindrer uønskede side-reaktioner mellem elektroden og elektro -
 Leviterende proteiner kan hjælpe med at diagnosticere opioidmisbrug, andre sygdommeProteiner skabte specifikke former, når de blev leviteret, som et smiley ansigt af lag. Kredit:Michigan State University Forskere ved Michigan State Universitys Precision Health Program har hjulpe
Leviterende proteiner kan hjælpe med at diagnosticere opioidmisbrug, andre sygdommeProteiner skabte specifikke former, når de blev leviteret, som et smiley ansigt af lag. Kredit:Michigan State University Forskere ved Michigan State Universitys Precision Health Program har hjulpe
- Er det muligt at optage lyd uden elektricitet?
- Hvad er den procentdel af energi, der bruges til at udføre arbejde, kaldet?
- Hvilken organisme kræver ikke sollys for at leve kemosyntetiske bakterier træer alger eller fotosy…
- Hvor findes oplysningerne til at dirigere en celle?
- Hvilke kræfter forårsager bevægelse opad i en plante?
- Ny undersøgelse viser den overraskende kraft i Wikipedia inden for videnskab


