Furan-reaktivitet:Forståelse af forskelle med pyrrol og thiophen
Faktorer, der bidrager til furans højere reaktivitet:
* iltens elektrondonerende evne: Iltatomet i furan er mere elektronegativt end nitrogen (pyrrol) eller svovl (thiophen). Dette gør det ensomme iltpar lettere tilgængeligt for donation til pi-systemet, hvilket øger elektrontætheden i ringen. Dette fører til en større modtagelighed for elektrofile angreb.
* Lavere aromaticitet: Furans aromaticitet er svagere sammenlignet med pyrrol og thiophen på grund af oxygenets højere elektronegativitet, hvilket destabiliserer ringsystemet. Dette gør furan mere tilbøjelig til reaktioner, der forstyrrer dets aromaticitet, såsom elektrofile angreb.
Det er dog her, sammenligningen bliver mere kompleks:
* Specifikke reaktioner: Mens furan er mere reaktiv i generelle elektrofile aromatiske substitutionsreaktioner (EAS), er det vigtigt at overveje de specifikke reaktionsbetingelser og elektrofilen. For eksempel gennemgår furan ringåbningsreaktioner meget lettere end pyrrol og thiophen , hvilket gør den mindre stabil i nogle tilfælde.
* Stabilitetsovervejelser: Pyrrol og thiophen nyder godt af den resonansstabilisering, som deres heteroatomer giver. De enlige par på nitrogen og svovl kan deltage i delokalisering, hvilket øger stabiliteten og reducerer reaktiviteten.
Samlet set:
Mens furan ofte beskrives som den mest reaktive af de tre heterocykler, er det afgørende at forstå, at dette afhænger af den reaktion, der overvejes, og de specifikke forhold. Hver heterocyklus har sin egen unikke reaktivitetsprofil, og en grundig forståelse af deres individuelle egenskaber er afgørende for at forudsige deres adfærd i forskellige kemiske miljøer.
 Varme artikler
Varme artikler
-
 Ved at opdage genetisk materiale, hurtig sensor har potentiel anvendelse som et klinisk værktøj3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License På mindre end et sekund, en lille sensor, der bruges i hjernekemiforskning, kan detektere nøglemolekylerne, der gi
Ved at opdage genetisk materiale, hurtig sensor har potentiel anvendelse som et klinisk værktøj3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License På mindre end et sekund, en lille sensor, der bruges i hjernekemiforskning, kan detektere nøglemolekylerne, der gi -
 Differentiering af alkoholer fra alkener i laboratoriet:en praktisk vejledningThinkstock/Stockbyte/Getty Images En alkohol indeholder en hydroxyl (-OH) funktionel gruppe, hvorimod en alken er defineret af en carbon-carbon dobbeltbinding. Hver funktionel gruppe deltager i forsk
Differentiering af alkoholer fra alkener i laboratoriet:en praktisk vejledningThinkstock/Stockbyte/Getty Images En alkohol indeholder en hydroxyl (-OH) funktionel gruppe, hvorimod en alken er defineret af en carbon-carbon dobbeltbinding. Hver funktionel gruppe deltager i forsk -
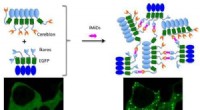 Se små molekylers interaktioner inde i cellerKredit:American Chemical Society Som mennesker i en stor virksomhed, proteiner i celler interagerer konstant med hinanden for at udføre forskellige job. At udvikle nye sygdomsbehandlinger, forsker
Se små molekylers interaktioner inde i cellerKredit:American Chemical Society Som mennesker i en stor virksomhed, proteiner i celler interagerer konstant med hinanden for at udføre forskellige job. At udvikle nye sygdomsbehandlinger, forsker -
 Molekyler, der bremser vildfarne proteiner af AL-amyloidose, peger på en ny type terapiKrystalstruktur af et antistofprotein fundet i letkædede amyloidoser, med succes stabiliseret af små molekyler identificeret i Kelly Lab. Kredit:Scripps Research Institute Forskere ved Scripps Res
Molekyler, der bremser vildfarne proteiner af AL-amyloidose, peger på en ny type terapiKrystalstruktur af et antistofprotein fundet i letkædede amyloidoser, med succes stabiliseret af små molekyler identificeret i Kelly Lab. Kredit:Scripps Research Institute Forskere ved Scripps Res
- Hvilken handling har mindst indflydelse på miljøet?
- Hvilken ældre videnskab eller teknologi?
- 100 hk lig med hvor mange mega watt?
- Hvad er målet for elektrisk energi, som en elektron bærer?
- I begyndelsen af det syttende århundrede spanske kontrollerede territorium, hvorpå kontinenter?
- Hvad er et blødt meget reaktivt metal?


