Molekyler, der bremser vildfarne proteiner af AL-amyloidose, peger på en ny type terapi
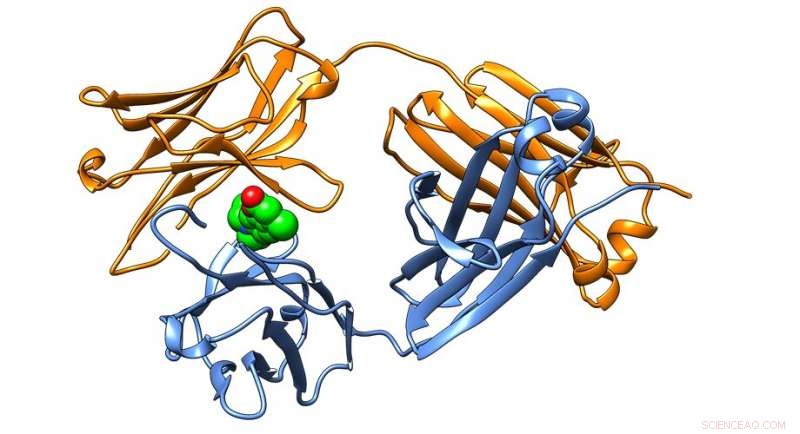
Krystalstruktur af et antistofprotein fundet i letkædede amyloidoser, med succes stabiliseret af små molekyler identificeret i Kelly Lab. Kredit:Scripps Research Institute
Forskere ved Scripps Research har identificeret en gruppe små molekyler, der forhindrer strukturelle ændringer af proteiner, der er roden til AL-amyloidose, en fremadskridende og ofte dødelig sygdom.
De små molekyler binder sig til immunglobulinproteiner, som spiller en væsentlig rolle i kroppens immunsystem, og derefter stabilisere underenheder af proteinet kaldet immunoglobulin lette kæder. Binding og stabilisering af de lette kæder i deres oprindelige form forhindrer dem i at folde forkert og danne de toksiske plaques, der findes hos patienter med AL-amyloidose.
Ved at mærke lette kæder med fluoroforer og koble formændringer til spaltning af proteinase K, næsten en million små molekyler blev screenet for deres evne til at forhindre de sygdomsassocierede strukturelle ændringer ved hjælp af fluorescenspolarisering. Ved at bruge denne strategi som grundlag for en high-throughput skærm og forskellige distinkte modskærme for at eliminere artefakter, holdet opdagede flere lægemiddelkandidater med små molekyler, der forhindrede immunglobulin-lette kæder i at folde sig forkert og aggregere i et reagensglas. Tilgangen, hvis det lykkes hos mennesker, kunne ændre sygdomsforløbet.
"Fordi vi har identificeret immunglobulinets lette kædes lille molekyle bindingssted, der bibringer stabilisering ved krystallografi, vi mener, at disse fund repræsenterer en plan for fremstilling af et tiltrængt lægemiddel til AL-amyloidose, " siger Scripps Research kemiprofessor Jeffery Kelly, Ph.D., der ledede forskningen. "Hvis vi kan blokere aggregeringen af nyligt udskilte lette kæder og forhindre dem i at blive nedbrudt til aggregeringstilbøjelige fragmenter, vi håber at bremse eller endda standse sygdomsprogression, især for de patienter, der udviser hjertepåvirkning."
Amyloidose er en sjælden og sandsynligvis underdiagnosticeret sygdom, der antager mange former. AL amyloidose, også kaldet let kæde amyloidose, er den næsthyppigste systemiske amyloidsygdom, med nogle 4, 500 nye tilfælde hvert år i USA
Plasmacellerne fra mennesker med AL-amyloidose producerer en komponent af antistoffer kendt som immunoglobulin-lette kæder, ofte i stedet for antistoffer, som følge af en plasmacellekræft. De lette kæder folder sig forkert og/eller klumper sig sammen til små fibre, der er giftige for organer. Over tid, disse såkaldte amyloidaflejringer forstyrrer gradvist en sund hjertefunktion, nyrer, leveren og andre dele af kroppen.
Scripps Researchs Gareth Morgan, Ph.D., hovedforfatter af undersøgelsen, understreger, at AL-patienter med organinvolvering, især hjertepåvirkning, er ofte for syge til at tåle kemoterapi. Håbet er, at kinetiske stabilisatorer af immunglobulin-lette kæder vil kunne tjene som en første behandling for disse patienter, så de i sidste ende kan tåle kemoterapi.
Scripps Research-teamets resultater vises i Proceedings of the National Academy of Sciences . Ud over at beskrive deres kinetiske stabiliseringstilgang til behandling af AL-amyloidose, forskerne siger, at de forestiller sig en ligetil metode til at identificere de patienter, der med størst sandsynlighed vil have gavn af behandlingen.
Kelly siger, at lægemiddelmekanismen, som holdet identificerede, er analog med et andet lægemiddel, der også stammer fra Scripps Research:Tafamidis, som stabiliserer proteinet transthyretin til behandling af den mest almindelige systemiske amyloidsygdom, der påvirker hjertet eller andre organer. Kelly opfandt tafamidis sammen med Evan Powers, Ph.D., til behandling af transthyretin amyloidoser. Nu ejet af Pfizer, tafamidis er godkendt i Europa under navnet Vyndaqel og blev for nylig indsendt til FDA til godkendelse i USA.
Nicholas Yan, en kandidatstuderende og medførsteforfatter på undersøgelsen, udvikler nu mere potente og selektive immunoglobulin let kæde kinetiske stabilisatorer med lægemiddellignende egenskaber til brug i mennesker, undersøgelser, der udføres i samarbejde med Reji Nair, Ph.D., en post-doc stipendiat, også i samarbejde med andre hos Scripps Research.
Sidste artikelNy metode kan føre til bedre in vivo lægemiddellevering
Næste artikelForskere karakteriserer molekylær sakse til plastaffald
 Varme artikler
Varme artikler
-
 En kemisk skræddersyet dragt til Alzheimers medicinProteinkrystaller af det humane enzym glutaminylcyclase og atomstruktur af den nye inhibitor. Kredit:Lisa-Marie Funk Med over 1,2 millioner mennesker berørt alene i Tyskland og over 50 millioner m
En kemisk skræddersyet dragt til Alzheimers medicinProteinkrystaller af det humane enzym glutaminylcyclase og atomstruktur af den nye inhibitor. Kredit:Lisa-Marie Funk Med over 1,2 millioner mennesker berørt alene i Tyskland og over 50 millioner m -
 Nyt stofbibliotek for at fremskynde søgningen efter aktive stofferTil studiet, enzymet endothiapepsin (grå) blev kombineret med molekyler fra fragmentbiblioteket. Analysen viser, at adskillige stoffer er i stand til at koble sig til enzymet (blå og orange molekyler)
Nyt stofbibliotek for at fremskynde søgningen efter aktive stofferTil studiet, enzymet endothiapepsin (grå) blev kombineret med molekyler fra fragmentbiblioteket. Analysen viser, at adskillige stoffer er i stand til at koble sig til enzymet (blå og orange molekyler) -
 Liste over alkaliske kemikalierAlkaliske eller basiske kemikalier har en lang historie med menneskelig brug, der tjener som et kemisk modsætning til syrer. Fra brug af calciumchlorid som kridt og natriumbicarbonat som bagepulver ti
Liste over alkaliske kemikalierAlkaliske eller basiske kemikalier har en lang historie med menneskelig brug, der tjener som et kemisk modsætning til syrer. Fra brug af calciumchlorid som kridt og natriumbicarbonat som bagepulver ti -
 Forskere afslører dynamisk kobling af stærk hydrogenbindingAbstrakt https://doi.org/10.1021/acs.jpclett.1c00168 Hydrogenbindinger (HBer), de vigtigste intermolekylære interaktioner, er iboende svingende i naturen. At belyse de dynamiske koblinger af hydr
Forskere afslører dynamisk kobling af stærk hydrogenbindingAbstrakt https://doi.org/10.1021/acs.jpclett.1c00168 Hydrogenbindinger (HBer), de vigtigste intermolekylære interaktioner, er iboende svingende i naturen. At belyse de dynamiske koblinger af hydr
- Fotoniske metasurfaces giver en ny legeplads for twistronics
- Gabon jonglerer med konkurrerende krav i kampen for at beskytte naturen
- Brug af magneter i vores daglige liv
- Tilgængeligheden af brint styrer den kemiske struktur af grafenoxid
- Forbedring af bæredygtigheden af fracking via innovationer inden for spildevandshåndtering
- Hemmeligheden bag 3D-grafen? Bare frys det


