Beregning af mol kulstof til hæmatitreaktion:en trin-for-trin guide
1. Skriv den afbalancerede kemiske ligning:
Reaktionen mellem kulstof (C) og hæmatit (Fe₂O₃) producerer jern (Fe) og kuldioxid (CO₂):
2 Fe203 + 3 C → 4 Fe + 3 C02
2. Beregn mol af hæmatit:
* Find den molære masse af hæmatit (Fe₂O₃):(2 * 55,845 g/mol Fe) + (3 * 16,00 g/mol O) =159,69 g/mol
* Divider massen af hæmatit med dens molære masse:580 g / 159,69 g/mol =3,63 mol Fe₂O₃
3. Bestem molforholdet ud fra den balancerede ligning:
* Den afbalancerede ligning viser, at 3 mol kulstof reagerer med 2 mol hæmatit.
4. Beregn de nødvendige mol kulstof:
* Indstil en andel:(3 mol C / 2 mol Fe₂O₃) =(x mol C / 3,63 mol Fe₂O₃)
* Løs for x:x =(3 mol C * 3,63 mol Fe₂O3) / 2 mol Fe₂O3 =5,45 mol C
Derfor skal du bruge 5,45 mol kulstof for at reagere med 580 g hæmatit.
Sidste artikelFluor Atomnummer:Forståelse af Fluors egenskaber
Næste artikelForståelse af fødevaresurere:Sikkerhed og håndtering
 Varme artikler
Varme artikler
-
 Nye materialer til at hjælpe med at stoppe lithium-ion-batteri, eksplosioner og forbedrer batteriet…Dette billede viser en høj ionisk ledende og fleksibel polymer komposit elektrolytfilm til lithium-ion batterier. Kredit:Purdue University Fra biler og fly til bærbare computere og e-cykler, lithi
Nye materialer til at hjælpe med at stoppe lithium-ion-batteri, eksplosioner og forbedrer batteriet…Dette billede viser en høj ionisk ledende og fleksibel polymer komposit elektrolytfilm til lithium-ion batterier. Kredit:Purdue University Fra biler og fly til bærbare computere og e-cykler, lithi -
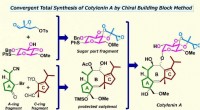 Total syntese af cotylenin A til et nyt kræftlægemiddel uden bivirkningerKredit:Nakada Laboratory, Waseda Universitet Det lykkedes for forskere ved Waseda University at udvikle en metode til en total syntese af cotylenin A, en plantevækstregulator, som har tiltrukket s
Total syntese af cotylenin A til et nyt kræftlægemiddel uden bivirkningerKredit:Nakada Laboratory, Waseda Universitet Det lykkedes for forskere ved Waseda University at udvikle en metode til en total syntese af cotylenin A, en plantevækstregulator, som har tiltrukket s -
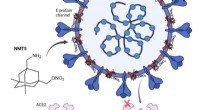 Nyt lægemiddel har potentiale til at vende SARS-CoV-2-virus mod sig selvEt lægemiddel udviklet af Scripps Research-forskere forhindrer SARS-CoV-2 (blå) i at binde sig til ACE2-receptorer (lyserøde) for at inficere menneskelige celler. Lægemidlet hæfter sig på virussen og
Nyt lægemiddel har potentiale til at vende SARS-CoV-2-virus mod sig selvEt lægemiddel udviklet af Scripps Research-forskere forhindrer SARS-CoV-2 (blå) i at binde sig til ACE2-receptorer (lyserøde) for at inficere menneskelige celler. Lægemidlet hæfter sig på virussen og -
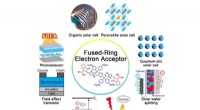 Fremskridt i elektronacceptorer med fusioneret ringStrukturen af ITIC og applikationer af FREAs. Kredit:College of Engineering, Peking Universitet Fra 1995-2015, fullerenderivater havde været de dominerende elektronacceptorer i organiske solcell
Fremskridt i elektronacceptorer med fusioneret ringStrukturen af ITIC og applikationer af FREAs. Kredit:College of Engineering, Peking Universitet Fra 1995-2015, fullerenderivater havde været de dominerende elektronacceptorer i organiske solcell
- Kunne den sagnomspundne Orientekspress gå på skinnerne igen?
- Liste over enkeltcelleorganismer
- I hvilken retning ville skyggen pege ved middagstid hver dag?
- Hvordan man bygger en robot, der efterligner dyrs bevægelser - og hvorfor du gerne vil
- Google-memo går fuldstændig glip af, hvordan implicitte skævheder skader kvinder
- 25-minutters test kunne forenkle indledende diagnose af urinvejsinfektioner, bekæmpe antibiotikares…


