Molekylære ligninger:Forståelse af støkiometri uden koefficienter
Her er hvorfor:
* Molekylær ligning: Viser de komplette kemiske formler for alle reaktanter og produkter, men angiver ikke deres relative mængder. Denne type ligning fokuserer på de involverede kemiske arter og deres overordnede transformation.
* Balanceret kemisk ligning: Inkluderer de støkiometriske koefficienter, der repræsenterer de relative mængder af hver reaktant og produkt involveret i reaktionen. Dette sikrer, at ligningen overholder loven om bevarelse af masse.
Eksempel:
Molekylær ligning:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l)
Balanceret kemisk ligning:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l)
Bemærk: Mens den molekylære ligning ikke viser støkiometrien, gør den afbalancerede kemiske ligning det (i dette tilfælde et forhold på 1:1:1:1).
 Varme artikler
Varme artikler
-
 Effektiv og high-throughput teknik til at studere strukturen af DNAFra venstre mod højre:SEM-billede af DNA-bundter homogent suspenderet over en superhydrofob enhed. I det relaterede HRTEM-billede har frynserne en afstand på 2,7 Å, i god overensstemmelse med diffrakt
Effektiv og high-throughput teknik til at studere strukturen af DNAFra venstre mod højre:SEM-billede af DNA-bundter homogent suspenderet over en superhydrofob enhed. I det relaterede HRTEM-billede har frynserne en afstand på 2,7 Å, i god overensstemmelse med diffrakt -
 Forskere udvikler en ny enhed til screening af avancerede krystallinske materialerVenstre til højre:Meenesh R. Singh (UIC), Paria Coliaie (UIC), Manish S. Kelkar (AbbVie Inc.) og Nandkishor K. Nere (AbbVie Inc.) viser nye mikrofluidiske enheder frem. Kredit:Meenesh Singh Forske
Forskere udvikler en ny enhed til screening af avancerede krystallinske materialerVenstre til højre:Meenesh R. Singh (UIC), Paria Coliaie (UIC), Manish S. Kelkar (AbbVie Inc.) og Nandkishor K. Nere (AbbVie Inc.) viser nye mikrofluidiske enheder frem. Kredit:Meenesh Singh Forske -
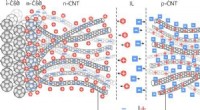 Forskere opdager overkommelig metode til produktion af transparente solcellerIonisk lukket lille-molekyle opv:grænseflade-doping af ladningssamler og transportlag. Kredit: ACS -anvendte materialer og grænseflader (2021). DOI:10.1021/acsami.0c17865 Fysikere fra ITMO Univ
Forskere opdager overkommelig metode til produktion af transparente solcellerIonisk lukket lille-molekyle opv:grænseflade-doping af ladningssamler og transportlag. Kredit: ACS -anvendte materialer og grænseflader (2021). DOI:10.1021/acsami.0c17865 Fysikere fra ITMO Univ -
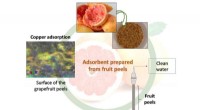 Spildevand renset takket være et nyt adsorberende materiale fremstillet af frugtskallerDiagram over processen designet af UGR-forskerne. Kredit:University of Granada Et samarbejde mellem forskere har udviklet en proces til at rense vand indeholdende tungmetaller og organiske foruren
Spildevand renset takket være et nyt adsorberende materiale fremstillet af frugtskallerDiagram over processen designet af UGR-forskerne. Kredit:University of Granada Et samarbejde mellem forskere har udviklet en proces til at rense vand indeholdende tungmetaller og organiske foruren
- Ny undersøgelse visualiserer bevægelse af vandmolekyler, lover ny bølge af elektroniske enheder
- Hvad er navnene og formlerne for oxysyrer jod?
- Sådan beregnes titrerbar surhed i vin:en trin-for-trin guide
- Hvilken videnskabelig metode følger eksperimentet?
- Hvilken retning handler jord gravitationskraft?
- Hvor hurtigt bevæger molekylerne sig for fast?


