Alkaliske jordmetaller:hvorfor de let mister elektroner
* Elektronisk konfiguration: Gruppe 2-elementer har to valenselektroner i deres yderste skal. Dette betyder, at de har en relativt ustabil konfiguration sammenlignet med en fuld ydre skal (som er meget stabil).
* Lav ioniseringsenergi: Ioniseringsenergi er den energi, der kræves for at fjerne en elektron fra et atom i dets gasformige tilstand. Gruppe 2-elementer har relativt lav ioniseringsenergi. Dette betyder, at det tager mindre energi at fjerne disse to valenselektroner, hvilket gør dem let tilgængelige for donation.
Hvorfor er det gunstigt at miste elektroner?
* Stabil oktet: Når gruppe 2-elementer mister deres to valenselektroner, opnår de en stabil oktetkonfiguration (8 elektroner i deres yderste skal), hvilket efterligner den elektroniske konfiguration af den nærmeste ædelgas. Dette gør dem mere stabile.
* Danning af kationer: Ved at miste elektroner danner gruppe 2-elementer positivt ladede ioner (kationer) med en ladning på +2. Dette giver dem mulighed for at danne ioniske bindinger med ikke-metaller, som har en tendens til at få elektroner.
Opsummering: Gruppe 2-elementer mister let deres to valenselektroner for at opnå en stabil elektronisk konfiguration og danne ionbindinger, hvilket fører til deres karakteristiske reaktivitet.
Sidste artikelLithiumsulfidanion:Forståelse af S²⁻-ionen
Næste artikelÆtsende syrer:typer, anvendelser og sikkerhed
 Varme artikler
Varme artikler
-
 Forskere udvikler 3D-printet geléHydrogelmaterialet kommer fra tangpartikler af forskellig størrelse. Kredit:Orlin Velev, NC State University 3D-printbare geler med forbedrede og meget kontrollerede egenskaber kan skabes ved at f
Forskere udvikler 3D-printet geléHydrogelmaterialet kommer fra tangpartikler af forskellig størrelse. Kredit:Orlin Velev, NC State University 3D-printbare geler med forbedrede og meget kontrollerede egenskaber kan skabes ved at f -
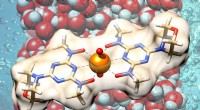 Bio-inspireret materiale retter sig mod oceanernes uranlagre for bæredygtig atomenergiVed at kombinere grundlæggende kemi med højtydende computerressourcer hos ORNL, forskere demonstrerer en mere effektiv metode til at genvinde uran fra havvand, afsløre et prototypemateriale, der overg
Bio-inspireret materiale retter sig mod oceanernes uranlagre for bæredygtig atomenergiVed at kombinere grundlæggende kemi med højtydende computerressourcer hos ORNL, forskere demonstrerer en mere effektiv metode til at genvinde uran fra havvand, afsløre et prototypemateriale, der overg -
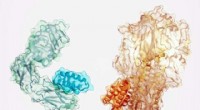 Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidlerSmå proteiner (mørkere nuance) designet til at binde sig til insulinreceptoren (venstre) og en komponent af influenzavirussen (højre). Kredit:Ian C. Haydon/Institute for Protein Design Et team af v
Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidlerSmå proteiner (mørkere nuance) designet til at binde sig til insulinreceptoren (venstre) og en komponent af influenzavirussen (højre). Kredit:Ian C. Haydon/Institute for Protein Design Et team af v -
 Kobberstearat lovende til tung olieoxidation, siger undersøgelseKredit:Kazan Federal University Kobbersalte har fundet plads i mange industrier fra lægemidler til landbrug, men de ses sjældent i petrokemi og olieudvinding. Nu, Forskere fra Kazan Federal Univer
Kobberstearat lovende til tung olieoxidation, siger undersøgelseKredit:Kazan Federal University Kobbersalte har fundet plads i mange industrier fra lægemidler til landbrug, men de ses sjældent i petrokemi og olieudvinding. Nu, Forskere fra Kazan Federal Univer
- Sådan komposterer du blade i en plastpose
- Hvilket stof har den største fordampningsvarme er det F2 Cl2 Br2 O2 I2?
- Hvilke forbindelser ville have de højeste kogepunkter?
- Hvilket område inden for biologisk videnskab giver det største potentiale for at forbedre menneske…
- Er ilt en gas opløst i havvand?
- Hvad er en konstellation, der giver tre eksempler?


