Xenon-Xenon-interaktioner:Forståelse af Londons spredningsstyrker
Her er hvorfor:
* Xenon er en ædelgas. Ædelgasser er monoatomiske, hvilket betyder, at de eksisterer som individuelle atomer snarere end molekyler.
* Londonske spredningskræfter er til stede i alle stoffer. Disse kræfter opstår fra midlertidige fluktuationer i elektronfordelingen omkring atomer eller molekyler, hvilket skaber midlertidige dipoler. Disse midlertidige dipoler kan inducere dipoler i tilstødende atomer eller molekyler, hvilket fører til svage attraktioner.
Mens xenon er et relativt stort atom med mange elektroner, er London-spredningskræfterne mellem to xenon-atomer stadig meget svage på grund af manglen på permanente dipoler og fraværet af andre intermolekylære kræfter som hydrogenbinding eller dipol-dipol-interaktioner.
 Varme artikler
Varme artikler
-
 Opdager den næste generation af katalysatorerProfessor Jan Rossmeisl Ved hjælp af to ph.d. -studerende Jack K. Pedersen og Thomas A.A. Batchelor. Kredit:Københavns Universitet Brugen af solenergi og vindenergi skal fordobles for at imødeko
Opdager den næste generation af katalysatorerProfessor Jan Rossmeisl Ved hjælp af to ph.d. -studerende Jack K. Pedersen og Thomas A.A. Batchelor. Kredit:Københavns Universitet Brugen af solenergi og vindenergi skal fordobles for at imødeko -
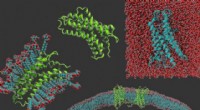 Forskere ændrer membranproteiner for at gøre dem nemmere at studereMed uret fra venstre:en g-proteinkoblet receptor i vaskemiddel, proteinet alene, en g-protein koblet receptor, der er blevet gjort vandopløselig, og g-proteinkoblede receptorer indlejret i en membran.
Forskere ændrer membranproteiner for at gøre dem nemmere at studereMed uret fra venstre:en g-proteinkoblet receptor i vaskemiddel, proteinet alene, en g-protein koblet receptor, der er blevet gjort vandopløselig, og g-proteinkoblede receptorer indlejret i en membran. -
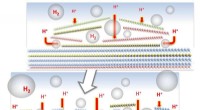 Bobler hjælper nye katalysatorer med at optimere sig selvEn elektrokatalysator skabt ved Rice University viste sig at være lige så effektiv som platin til produktion af brint. Processen skaber brintbobler mellem planer af det lagdelte materiale, som bryder
Bobler hjælper nye katalysatorer med at optimere sig selvEn elektrokatalysator skabt ved Rice University viste sig at være lige så effektiv som platin til produktion af brint. Processen skaber brintbobler mellem planer af det lagdelte materiale, som bryder -
 Kemikere foreslår ny gavnlig katalysator til indledende materialer i apoteketCyanosilylering af aldehyder. Kredit:Atash Gurbanov Et samarbejde mellem forskere fra RUDN University (Rusland), Centro de Química Estrutura (Portugal) og Baku State University (Aserbajdsjan) fore
Kemikere foreslår ny gavnlig katalysator til indledende materialer i apoteketCyanosilylering af aldehyder. Kredit:Atash Gurbanov Et samarbejde mellem forskere fra RUDN University (Rusland), Centro de Química Estrutura (Portugal) og Baku State University (Aserbajdsjan) fore
- Anmeldelse:Ingen nyt Apple TV? Prøv Nvidia Shield i stedet
- Ny software har til formål at gøre videnskaben mere replikerbar
- Forskere laver grafenhybrid
- Match strukturen i kolonne 1 til egenskaber 2 En moho -barriere tyndeste lag B oceanisk skorpe, der …
- Global opvarmning i dag afspejler forhold, der fører til Jordens største udryddelsesbegivenhed, si…
- Hvilken type måling er 10 Newton?


