Stærke syrer vs. stærke baser:Forstå deres styrke
Her er en oversigt:
Stærk vs. svag:
* Stærke syrer og baser ionisere fuldstændigt i opløsning, hvilket betyder, at de dissocierer til deres ioner 100%.
* Svage syrer og baser kun delvist ionisere i opløsning, hvilket betyder, at kun en lille del af deres molekyler nedbrydes til ioner.
Derfor, hvad angår ionisering, er en stærk syre lige så "stærk" som en stærk base. Begge vil dissociere fuldstændigt til ioner, bare med forskellige typer ioner (H+ for syrer og OH- for baser).
Men der er mere i det end bare ionisering:
* Styrke relaterer sig også til reaktivitet. En stærk syre er generelt mere reaktiv end en svag syre, og det samme gælder for baser.
* pH-skala: pH-skalaen måler surhedsgraden eller alkaliniteten af en opløsning. En lavere pH indikerer en højere koncentration af H+ ioner (sure), mens en højere pH indikerer en højere koncentration af OH- ioner (alkaliske).
Så, hvad der er "stærkere" afhænger i sidste ende af konteksten:
* Med hensyn til ionisering: En stærk syre og en stærk base er lige stærke.
* Med hensyn til reaktivitet: Stærke syrer og baser er generelt mere reaktive end deres svage modstykker.
* Med hensyn til pH: En stærk syre vil have en lavere pH end en stærk base.
Det er vigtigt at huske, at både stærke syrer og baser kan være farlige og kræver omhyggelig håndtering.
 Varme artikler
Varme artikler
-
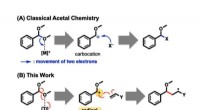 Radikal kemi muliggør ligetil syntese af ethereFigur 1. Aktiveringstilstand for acetaler. (A) Klassisk, acetal C-O-bindinger spaltes på heterolytisk vis. To elektroner, der udgør en C-O-binding, fjernes begge af en sur aktivator ([M]+) for at tilv
Radikal kemi muliggør ligetil syntese af ethereFigur 1. Aktiveringstilstand for acetaler. (A) Klassisk, acetal C-O-bindinger spaltes på heterolytisk vis. To elektroner, der udgør en C-O-binding, fjernes begge af en sur aktivator ([M]+) for at tilv -
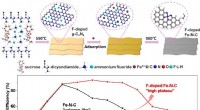 Forskere bruger fluor-dopingmetode til at konstruere katalysatorer med forbedret ydeevneDen F-dopede Fe-N-C enkeltstedskatalysator bevarer fordelen ved lavt overpotentiale for Fe-N-C med meget øget CO faradaisk effektivitet og delvis strømtæthed på grund af den stabiliserede Fe3+ aktive
Forskere bruger fluor-dopingmetode til at konstruere katalysatorer med forbedret ydeevneDen F-dopede Fe-N-C enkeltstedskatalysator bevarer fordelen ved lavt overpotentiale for Fe-N-C med meget øget CO faradaisk effektivitet og delvis strømtæthed på grund af den stabiliserede Fe3+ aktive -
 Mulige nye antivirale midler mod COVID-19, herpesPeptoider (blå, venstre) gennembore beskyttelseslaget af en virus, forårsager dens opløsning og inaktivering (til højre). Kredit:Maxwell Biosciences Ud over antistoffer og hvide blodlegemer, immun
Mulige nye antivirale midler mod COVID-19, herpesPeptoider (blå, venstre) gennembore beskyttelseslaget af en virus, forårsager dens opløsning og inaktivering (til højre). Kredit:Maxwell Biosciences Ud over antistoffer og hvide blodlegemer, immun -
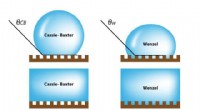 Forståelse af overfladevidenskab til fremstilling af kosmetik af høj kvalitetBefugtningsovergangen fra Cassie-Baxter-tilstand til Wenzel-tilstand på strukturerede overflader. Kredit:UNIST Et forskerhold tilknyttet UNIST har undersøgt hastighederne for væskepenetration på r
Forståelse af overfladevidenskab til fremstilling af kosmetik af høj kvalitetBefugtningsovergangen fra Cassie-Baxter-tilstand til Wenzel-tilstand på strukturerede overflader. Kredit:UNIST Et forskerhold tilknyttet UNIST har undersøgt hastighederne for væskepenetration på r
- Impulsiv spiser? At huske fejl kan hjælpe med at bremse spisningen
- Hvad er navnene på forskellige tåge?
- Tall Whites:The Classic Alien Archetype Explained
- Henfalder protoner? Svaret kan være på månen
- Hvilken gruppe i det periodiske system indeholder flest reaktive ikke-metaller?
- Amazon Echo Show 15 anmeldelse:Er al den skærmplads det værd for 249,99 USD?


