Forståelse af pH 10 i kompleksometriske EDTA-titreringer
Hvorfor kompleksometriske titreringer?
* Metalionbestemmelse: Kompleksometriske titreringer bruges til at bestemme koncentrationen af metalioner i opløsning.
* EDTA som chelaterende agent: EDTA er et kraftigt chelaterende middel, hvilket betyder, at det kan binde sig til metalioner og danne stabile komplekser.
Hvorfor pH 10?
1. EDTA-stabilitet: EDTA er en svag syre, og dens evne til at binde sig til metalioner er pH-afhængig. Ved en højere pH eksisterer EDTA primært i sin deprotonerede form, som er den form, der effektivt binder metalioner.
2. Metalhydroxiddannelse: Ved lavere pH kan metalioner danne uopløselige hydroxidudfældninger. Dette ville forstyrre titreringen, da EDTA'en ikke kan binde sig til metalionerne, hvis de udfældes.
3. Buffering: En pH-værdi på 10 opretholdes sædvanligvis under anvendelse af en bufferopløsning. Dette sikrer, at pH-værdien forbliver stabil under titreringen, hvilket forhindrer eventuelle skift i ligevægten mellem EDTA og metalionerne.
4. Optimale reaktionsbetingelser: For mange metalioner giver pH-området omkring 10 de bedst egnede betingelser for både dannelsen af EDTA-metalkomplekset og forebyggelse af hydroxidudfældning.
Eksempler:
* Titrering af calcium med EDTA: Ved en pH på 10 dannes EDTA-calciumkomplekset, og calciumhydroxidudfældning undgås.
* Titrering af magnesium med EDTA: I lighed med calcium er opretholdelse af en pH på 10 ideel til at danne EDTA-magnesiumkomplekset.
Nøglepunkter:
* Den optimale pH for en kompleksometrisk titrering kan variere afhængigt af den specifikke metalion, der bestemmes.
* pH-justeringer kan være nødvendige for at sikre de bedste resultater.
* Indikatorer bruges til visuelt at detektere slutpunktet for titreringen, hvor alle metalionerne har reageret med EDTA.
Vigtig bemærkning: Henvis altid til specifikke analytiske metoder og procedurer for de præcise pH-krav til din bestemte titrering.
 Varme artikler
Varme artikler
-
 Udskrivning af trådløst genopladelige solid-state superkapacitorer til bløde, smarte kontaktlinse…DIW-baseret fremstilling og karakterisering af MIS-superkapacitoren. (A) Skematisk af den smarte kontaktlinse og DIW-baserede fremstillingsproces af den monolitisk integrerede MIS-superkapacitor med e
Udskrivning af trådløst genopladelige solid-state superkapacitorer til bløde, smarte kontaktlinse…DIW-baseret fremstilling og karakterisering af MIS-superkapacitoren. (A) Skematisk af den smarte kontaktlinse og DIW-baserede fremstillingsproces af den monolitisk integrerede MIS-superkapacitor med e -
 Forskere studerer tilstedeværelsen af fluorholdige kemikalier i brandmandstøjKredit:CC0 Public Domain Forskere ved University of Notre Dame vil begynde en uafhængig undersøgelse af deltagelsesudstyr, der bæres af brandmænd, efter at de første prøver blev testet positivt fo
Forskere studerer tilstedeværelsen af fluorholdige kemikalier i brandmandstøjKredit:CC0 Public Domain Forskere ved University of Notre Dame vil begynde en uafhængig undersøgelse af deltagelsesudstyr, der bæres af brandmænd, efter at de første prøver blev testet positivt fo -
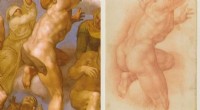 Ny hydrogel udviklet til at fjerne tape fra århundreder gammel tegning(Venstre) Detalje fra Ascesa dei Beati (Michelangelo Buonarroti) fra Det Sixtinske Kapel; (Til højre) tegning fra 1500-tallet, der gengiver den samme detalje. En indskrift di mano di Michelangelo (fra
Ny hydrogel udviklet til at fjerne tape fra århundreder gammel tegning(Venstre) Detalje fra Ascesa dei Beati (Michelangelo Buonarroti) fra Det Sixtinske Kapel; (Til højre) tegning fra 1500-tallet, der gengiver den samme detalje. En indskrift di mano di Michelangelo (fra -
 Hvor godt match er det? Lægger statistik ind i retsmedicinsk skydevåbenidentifikationWilmer Souder, en fysiker og tidlig retsmediciner ved National Bureau of Standards, nu NIST, sammenligner to kugler ved hjælp af et sammenligningsmikroskop. Souder lærte retsmedicinske teknikker af Ca
Hvor godt match er det? Lægger statistik ind i retsmedicinsk skydevåbenidentifikationWilmer Souder, en fysiker og tidlig retsmediciner ved National Bureau of Standards, nu NIST, sammenligner to kugler ved hjælp af et sammenligningsmikroskop. Souder lærte retsmedicinske teknikker af Ca
- Hvad er det grundlæggende princip for kinetisk teori?
- Forskning afslører, hvordan vulkanudbrud påvirker El Niño
- Funker internationale traktater rent faktisk? Undersøgelse siger, at de for det meste ikke
- Hvad er kraften mellem en elektron og kerne i et hydrogenatom?
- Vil folk gøre, som de får besked på?
- Styring af kemiske reaktioner nær det absolutte nul


