Tegning af kemiske strukturer:En omfattende vejledning
1. Forstå det grundlæggende
* Atomer: De grundlæggende byggesten i al materie. De består af en kerne (indeholdende protoner og neutroner) og elektroner, der kredser om kernen.
* Elementer: Rene stoffer, der kun består af én type atom (f.eks. brint, kulstof, oxygen).
* Forbindelser: Stoffer dannet, når to eller flere forskellige grundstoffer kombineres kemisk (f.eks. vand, kuldioxid).
* Kemiske formler: Repræsenter typerne og antallet af atomer i en forbindelse (f.eks. H2O for vand, CO2 for kuldioxid).
2. Bestem elementerne og deres antal
* Kemisk formel: Start med den kemiske formel for forbindelsen. Dette fortæller dig, hvilke typer af elementer der er til stede og deres mængder.
* Eksempel: Vand (H2O) har to hydrogenatomer (H) og et oxygenatom (O).
3. Forstå binding
* Kovalent binding: Atomer deler elektroner for at opnå en stabil elektronkonfiguration. Dette er den mest almindelige type binding i organiske forbindelser.
* Ionisk binding: Et atom overfører elektroner til et andet og skaber ioner med modsatte ladninger, der tiltrækker hinanden. Dette er almindeligt i uorganiske forbindelser.
4. Tegn skeletstrukturen
* Centralatom: Ofte vil det mindst elektronegative atom (atomet med den lavere tendens til at tiltrække elektroner) være det centrale atom.
* Forbindelse: Forbind atomerne i forbindelsen baseret på den kemiske formel og bindingsregler.
* Eksempel: I metan (CH4) er kulstof (C) det centrale atom, og det er bundet til fire hydrogenatomer (H).
5. Tilføj elektroner og ensomme par
* Valenselektroner: Antallet af elektroner i den yderste skal af et atom.
* Oktetregel: De fleste atomer stræber efter at have otte elektroner i deres yderste skal (undtagelser:brint og helium).
* Ensomme par: Elektronpar, der ikke er involveret i binding. Disse er ofte tegnet som prikker omkring et atom.
6. Overvej molekylær geometri
* Form: Arrangementet af atomer i tredimensionelt rum. Molekylær geometri påvirker forbindelsens egenskaber.
* VSEPR-teori: Denne teori hjælper med at forudsige molekylære former baseret på frastødning af elektronpar.
Eksempel:Tegning af vandets atomare struktur (H₂O)
1. Kemisk formel: H2O
2. Elementer: Brint (H) og ilt (O)
3. Binding: Kovalent binding (deling af elektroner)
4. Skelet: O i midten, forbundet med to H-atomer.
5. Elektroner: Ilt har 6 valenselektroner, brint har 1. Ilt danner to kovalente bindinger med brint og efterlader 2 ensomme elektronpar på oxygenatomet.
6. Molekylær geometri: Vand har en bøjet form på grund af frastødningen mellem de enlige par og bindende elektronpar.
Tips til tegning af atomare strukturer:
* Brug en blyant: Dette giver mulighed for nem sletning og rettelser.
* Brug en lige kant: For præcise linjer.
* Mærk atomer og bindinger: Dette hjælper dig med at holde styr på strukturen.
* Øv: At tegne atomare strukturer kræver øvelse. Start med simple forbindelser og arbejd gradvist mod mere komplekse.
* Ressourcer: Brug lærebøger, online tutorials og andre ressourcer til at lære mere om atomare strukturer og binding.
Softwareværktøjer
* ChemDraw: Kraftig software til tegning af kemiske strukturer.
* MarvinSketch: Gratis online tegneværktøj.
Husk, at tegne atomstrukturen af en forbindelse er en væsentlig færdighed i kemi. Ved at forstå det grundlæggende og øve dig, kan du trygt repræsentere strukturen af forskellige molekyler.
 Varme artikler
Varme artikler
-
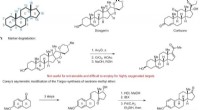 Strømlinet proces åbner lægemiddeludvikling til en ny klasse af steroiderIntroduktion til steroidstruktur og syntese. en, Det generelle steroid tetracykliske skelet. b, Eksempler på naturlige steroider. c, Udvalgte metoder til steroidsyntese ved hjælp af semisyntetiske og
Strømlinet proces åbner lægemiddeludvikling til en ny klasse af steroiderIntroduktion til steroidstruktur og syntese. en, Det generelle steroid tetracykliske skelet. b, Eksempler på naturlige steroider. c, Udvalgte metoder til steroidsyntese ved hjælp af semisyntetiske og -
 Intelligent genvinding og genbrug af balsatræOmkring 20 procent af elektriciteten i Tyskland blev produceret af vindmøller i 2018. Kredit:Hans-Peter Merten/MATOfoto Der er 30, 000 vindmøller i drift i Tyskland, hvoraf mange begynder at ældes
Intelligent genvinding og genbrug af balsatræOmkring 20 procent af elektriciteten i Tyskland blev produceret af vindmøller i 2018. Kredit:Hans-Peter Merten/MATOfoto Der er 30, 000 vindmøller i drift i Tyskland, hvoraf mange begynder at ældes -
 NRL pigmentpakke til skibe bremser misfarvning, sænker soltemperaturbelastningenNRL arbejder i øjeblikket med Naval Sea Systems Command, Naval Systems Engineering Directorate, Ship Integrity &Performance Engineering (SEA 05P) for at overføre den nye pigmentkombination til en mili
NRL pigmentpakke til skibe bremser misfarvning, sænker soltemperaturbelastningenNRL arbejder i øjeblikket med Naval Sea Systems Command, Naval Systems Engineering Directorate, Ship Integrity &Performance Engineering (SEA 05P) for at overføre den nye pigmentkombination til en mili -
 Mekanismer for bevaring af blødt væv og protein i Tyrannosaurus rexEt fossilt eksemplar af T. rex (AMNH 5027) udstillet på American Museum of Natural History, i 2019. Kredit:Nationalmuseet for Naturhistorisk, New York City. amnh.org/exhibitions/permanent/saurischian-
Mekanismer for bevaring af blødt væv og protein i Tyrannosaurus rexEt fossilt eksemplar af T. rex (AMNH 5027) udstillet på American Museum of Natural History, i 2019. Kredit:Nationalmuseet for Naturhistorisk, New York City. amnh.org/exhibitions/permanent/saurischian-


