Argonforbindelser:Udforskning af sjældne og ustabile kemiske arter
1. Argonfluorhydrid (HArF) :Dette er en meget ustabil forbindelse dannet under højt tryk og lav temperatur. Det er den eneste kendte neutrale forbindelse af argon.
2. Argonhydridion (ArH+) :Dette er en kationisk art observeret i det interstellare medium og laboratorieeksperimenter.
3. Argonfluoridion (ArF-) :Dette er en anionisk art observeret i laboratorieforsøg.
4. Argonkomplekser :Argon kan danne svage, forbigående komplekser med andre molekyler, især med meget polære molekyler som vand. Disse er ikke ægte kemiske forbindelser, men snarere kortvarige interaktioner.
5. Argon-klatrater :Argon kan fanges i burene af visse krystallinske strukturer kaldet clathrates. Disse er ikke kemiske forbindelser, men snarere fysiske blandinger.
Det er vigtigt at bemærke, at disse forbindelser er ekstremt sjældne og ustabile, hvilket gør dem udfordrende at studere og ikke relevante til hverdagsbrug. Argon bruges primært i sin elementære form til forskellige formål, såsom inerte atmosfærer ved svejsning og fremstilling, og belysning i lysstofrør.
Sidste artikelForståelse af kovalente bindinger i vand (H₂O)
Næste artikelJern og silicium:elementer vs. forbindelser - en klar forklaring
 Varme artikler
Varme artikler
-
 4 gennemprøvede strategier til at fremskynde kemiske reaktionerAf Vaibhav Rakesh – Opdateret 30. august 2022 Totojang/iStock/GettyImages En kemisk reaktion er drevet af kollisioner mellem reaktantmolekyler. En reaktions hastighed kan øges ved at manipulere fle
4 gennemprøvede strategier til at fremskynde kemiske reaktionerAf Vaibhav Rakesh – Opdateret 30. august 2022 Totojang/iStock/GettyImages En kemisk reaktion er drevet af kollisioner mellem reaktantmolekyler. En reaktions hastighed kan øges ved at manipulere fle -
 Polystyren vs. polyurethan:nøgleforskelle i sammensætning, termisk og kemisk ydeevneAf Robert Paxton, Opdateret 24. marts 2022 Polystyren og polyurethan er to udbredte syntetiske polymerer, hver med forskellige egenskaber, der gør dem velegnede til forskellige anvendelser. Mens poly
Polystyren vs. polyurethan:nøgleforskelle i sammensætning, termisk og kemisk ydeevneAf Robert Paxton, Opdateret 24. marts 2022 Polystyren og polyurethan er to udbredte syntetiske polymerer, hver med forskellige egenskaber, der gør dem velegnede til forskellige anvendelser. Mens poly -
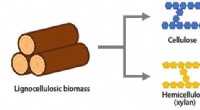 Ny metabolisk ingeniørstrategi forbedrer bioproduktion af polymerråmaterialerFigur 1:Strukturelle komponenter af lignocelluloseholdig biomasse (som ikke konkurrerer med globale fødevareforsyninger). Kredit:Kobe University En forskergruppe, bestående af doktorand Fujiwara R
Ny metabolisk ingeniørstrategi forbedrer bioproduktion af polymerråmaterialerFigur 1:Strukturelle komponenter af lignocelluloseholdig biomasse (som ikke konkurrerer med globale fødevareforsyninger). Kredit:Kobe University En forskergruppe, bestående af doktorand Fujiwara R -
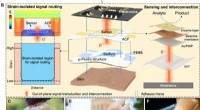 En bærbar, fritstående elektrokemisk sensorsystemFESS design begrundelse, implementering, og ansøgning. (A) skematisk af biomarkørinformationsleveringsvejen aktiveret af FESS, illustrerer prøveudtagning, sansning, og routing af epidermalt hentet bio
En bærbar, fritstående elektrokemisk sensorsystemFESS design begrundelse, implementering, og ansøgning. (A) skematisk af biomarkørinformationsleveringsvejen aktiveret af FESS, illustrerer prøveudtagning, sansning, og routing af epidermalt hentet bio
- 430 millioner år gammel uddød pighud fundet i England
- E-affaldsspisende protein skaber sjældne jordarter
- Hvad er en kraft, der former jordsinden ved at opbygge bjerge og landmasser?
- Ny forskning afslører, hvordan galakser undgår tidlig død
- Sådan bruges kobber til at lave din egen EMF-protektor
- Hvad er resultatet af, at solen er direkte over ækvator den 21. marts?


