Hydrogenbinding:Ioniske og kovalente interaktioner forklaret
Her er en oversigt:
Ionisk binding:
* Brint danner typisk ioniske bindinger med stærkt elektronegative elementer som halogener (F, Cl, Br, I), oxygen (O) og nitrogen (N) .
* I disse bindinger mister brint sin enkeltelektron og danner en positivt ladet hydrogenion (H+) . Denne ion tiltrækker så de negativt ladede ioner af det andet element.
Kovalent binding:
* Hydrogen danner kovalente bindinger med grundstoffer, der har lignende elektronegativitetsværdier, såsom carbon (C), phosphor (P), svovl (S) og andre brintatomer .
* I kovalente bindinger deler brint sin enkeltelektron med det andet element, hvilket skaber et fælles elektronpar. Dette delte par tiltrækkes af kernerne i begge atomer og holder dem sammen.
Eksempler på hydrogenbinding:
* Vand (H2O): Hydrogen danner kovalente bindinger med oxygen.
* Metan (CH4): Hydrogen danner kovalente bindinger med kulstof.
* Saltsyre (HCl): Hydrogen danner en ionbinding med klor.
* Ammoniak (NH3): Hydrogen danner kovalente bindinger med nitrogen.
Vigtig bemærkning: Brint kan også danne metalliske bindinger i nogle metalliske hydrider.
Nøglepunkt: Den type binding, der dannes mellem brint og et andet grundstof, afhænger af forskellen i deres elektronegativitet.
 Varme artikler
Varme artikler
-
 Uber medicin levering til kræftpatienterPh.d.-kandidaterne Samantha Wade og Sepehr Talebian, Dr Javad Foroughi, Fornemme professor Gordon Wallace og Dr. Kara Vine-Perrow. Kredit:Alex Pike Kræft er fortsat en af de største dødsårsager
Uber medicin levering til kræftpatienterPh.d.-kandidaterne Samantha Wade og Sepehr Talebian, Dr Javad Foroughi, Fornemme professor Gordon Wallace og Dr. Kara Vine-Perrow. Kredit:Alex Pike Kræft er fortsat en af de største dødsårsager -
 Samling af store videnskabelige værktøjer til at kaste lys over fleksible proteinerL-R:ORNLs Arvind Ramanathan, Hugh ONeill, og Paul Gilna inde i Summit supercomputerrummet. Kredit:Oak Ridge National Laboratory Næsten et dusin videnskabsmænd på tværs af Oak Ridge National Labora
Samling af store videnskabelige værktøjer til at kaste lys over fleksible proteinerL-R:ORNLs Arvind Ramanathan, Hugh ONeill, og Paul Gilna inde i Summit supercomputerrummet. Kredit:Oak Ridge National Laboratory Næsten et dusin videnskabsmænd på tværs af Oak Ridge National Labora -
 Forskere afkoder dynamikken i den største proteinnedbrydende maskine i atomare detaljerKredit:CC0 Public Domain Protein nanomaskiner lavet af flere proteinmolekyler er meget dynamiske under deres handlinger på deres funktionelle mål, nogle gange kaldet substrater. Dynamikken af di
Forskere afkoder dynamikken i den største proteinnedbrydende maskine i atomare detaljerKredit:CC0 Public Domain Protein nanomaskiner lavet af flere proteinmolekyler er meget dynamiske under deres handlinger på deres funktionelle mål, nogle gange kaldet substrater. Dynamikken af di -
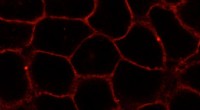 Hvordan forskere analyserer cellemembranerEn ny forbindelse, der efterligner naturligt kolesterol i membraner af levende celler (her:HeLa-celler). Stoffet er mærket med et fluorescerende farvestof (rødt). Kredit:L. Rakers et al./ Cell Chem B
Hvordan forskere analyserer cellemembranerEn ny forbindelse, der efterligner naturligt kolesterol i membraner af levende celler (her:HeLa-celler). Stoffet er mærket med et fluorescerende farvestof (rødt). Kredit:L. Rakers et al./ Cell Chem B


