Acetylen og dinitrogenoxidreaktion:ligning, produkter og forklaring
Her er en forenklet fremstilling af reaktionen, som fokuserer på de primære produkter:
C2H2 + 2 N2O → 2 CO2 + H2O + 2 N2
Forklaring:
* Acetylen (C2H2): Brændstofkilden.
* Nitrogenoxid (N₂O): Oxidationsmidlet, der giver ilten til forbrænding.
* Carbondioxid (CO₂): Det primære produkt af forbrændingen af kulstofatomerne i acetylen.
* Vand (H₂O): Det primære produkt af forbrændingen af hydrogenatomerne i acetylen.
* Nitrogen (N₂): Produktet af nedbrydning af dinitrogenoxid.
Vigtige overvejelser:
* Forbrændingstemperatur: Reaktionen kræver en høj temperatur for at starte. Dette opnås typisk ved at bruge en gnist eller flamme.
* Reaktionsmekanisme: Den faktiske mekanisme er mere kompleks og involverer flere mellemliggende trin, hvilket potentielt fører til dannelsen af andre produkter som nitrogenoxider (NOx).
* Stykiometri: Det nøjagtige forhold mellem reaktanter, der er nødvendige for fuldstændig forbrænding, kan variere lidt afhængigt af reaktionsbetingelserne.
Applikationer:
Denne reaktion er almindeligt anvendt i:
* Gasvejsning: Acetylen og dinitrogenoxid bruges som brændstof-oxidationsmiddel i svejseprocesser.
* Gasskæring: Den høje temperatur, der genereres af denne reaktion, kan bruges til at skære metaller.
Husk, at dette er en forenklet fremstilling, og at den faktiske reaktion er mere indviklet. For specifikke applikationer og detaljerede analyser er det vigtigt at rådføre sig med eksperter eller omfattende kemiteknisk litteratur.
 Varme artikler
Varme artikler
-
 Bedre kemi gennem bittesmå antennerKredit:CC0 Public Domain Et forskerhold ved University of Tokyo har introduceret en kraftfuld metode til aktivt at bryde kemiske bindinger ved hjælp af excitationer i bittesmå antenner skabt af in
Bedre kemi gennem bittesmå antennerKredit:CC0 Public Domain Et forskerhold ved University of Tokyo har introduceret en kraftfuld metode til aktivt at bryde kemiske bindinger ved hjælp af excitationer i bittesmå antenner skabt af in -
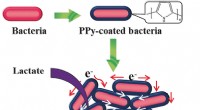 Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s
Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s -
 Design af fleksible og strækbare elektroniske enkeltkrystalsystemerYing Diao er interesseret i at udvikle teknikker, der hjælper med fremstilling af elektroniske materialer, energiudstyr, og terapeutiske modeller. Kredit:L. Brian Stauffer, University of Illinois i Ur
Design af fleksible og strækbare elektroniske enkeltkrystalsystemerYing Diao er interesseret i at udvikle teknikker, der hjælper med fremstilling af elektroniske materialer, energiudstyr, og terapeutiske modeller. Kredit:L. Brian Stauffer, University of Illinois i Ur -
 Mere solenergi takket være titaniumKredit:Wiley Jord rigeligt, billige metaller er lovende fotokatalytiske elektrodematerialer i kunstig fotosyntese. Et hold kinesiske forskere rapporterer nu, at et tyndt lag titaniumdioxid under h
Mere solenergi takket være titaniumKredit:Wiley Jord rigeligt, billige metaller er lovende fotokatalytiske elektrodematerialer i kunstig fotosyntese. Et hold kinesiske forskere rapporterer nu, at et tyndt lag titaniumdioxid under h
- Mennonitter gjorde Paraguay til en mega oksekødsproducent:Nu skal oprindelige folk betale prisen
- Sådan fungerer NASA Planetary Protection
- Smarte bandager designet til at overvåge og skræddersy behandling til kroniske sår
- Ny undersøgelse anslår CO2-fodsporene på 13, 000 byer
- Lyft taber penge igen, men ser overskud om cirka 2 år
- Plantebaserede magnetiske nanopartikler med svampedræbende egenskaber


