Hydrogenbinding:Identifikation af molekyler, der ikke danner denne interaktion
Forståelse af hydrogenbinding
Hydrogenbinding er en speciel type dipol-dipol-interaktion, der opstår, når:
1. Brint (H) er direkte bundet til et stærkt elektronegativt atom (som oxygen (O), nitrogen (N) eller fluor (F)).
2. Brintatomet tiltrækkes af et ensomt elektronpar på et andet stærkt elektronegativt atom i et nærliggende molekyle.
Eksempler:
* Vand (H₂O): H-atomerne er bundet til O, og O har enlige par, så vand danner stærke brintbindinger.
* Ammoniak (NH₃): H-atomerne er bundet til N, og N har et ensomt par, hvilket muliggør hydrogenbinding.
* Methanol (CH₃OH): H-atomet knyttet til O'et kan danne hydrogenbindinger.
Molekylet, der ikke vil udvise hydrogenbinding
Molekylet, der ikke vil udvise hydrogenbinding er methan (CH4) .
Her er hvorfor:
* Ingen højelektronegative atomer: Metan har kun kulstof- og brintatomer. Ingen af disse elementer er meget elektronegative.
* Ingen ensomme par: Kulstofatomet i metan har ikke nogen ensomme elektronpar til at deltage i hydrogenbinding.
Sig til, hvis du vil udforske flere eksempler!
 Varme artikler
Varme artikler
-
 Biologisk nedbrydelig plast fra palmeolieaffaldKredit:CC0 Public Domain En bionedbrydelig film lavet af affald fra palmeolieindustrien kunne bruges til fødevareemballage Plastforurening er et presserende miljøproblem i det enogtyvende århundr
Biologisk nedbrydelig plast fra palmeolieaffaldKredit:CC0 Public Domain En bionedbrydelig film lavet af affald fra palmeolieindustrien kunne bruges til fødevareemballage Plastforurening er et presserende miljøproblem i det enogtyvende århundr -
 Forskere udvikler diagnostisk værktøj til påvisning af cryptosporidiumIngeniørdoktorand George Luka siger, at der er et presserende behov for at udvikle en hurtig, fleksibel, nøjagtigt og realtidsdetektionsværktøj til at klare udfordringen med at beskytte vandforbrugere
Forskere udvikler diagnostisk værktøj til påvisning af cryptosporidiumIngeniørdoktorand George Luka siger, at der er et presserende behov for at udvikle en hurtig, fleksibel, nøjagtigt og realtidsdetektionsværktøj til at klare udfordringen med at beskytte vandforbrugere -
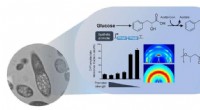 Et-trins produktion af aromatiske polyestere af E. coli-stammerBiosyntese af aromatiske polyestere ved metabolisk manipuleret E coli .Dette skematiske diagram viser den overordnede konceptualisering af, hvordan metabolisk manipuleret E coli fremstillet aromat
Et-trins produktion af aromatiske polyestere af E. coli-stammerBiosyntese af aromatiske polyestere ved metabolisk manipuleret E coli .Dette skematiske diagram viser den overordnede konceptualisering af, hvordan metabolisk manipuleret E coli fremstillet aromat -
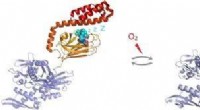 S-glutathionylering af human-inducerbar Hsp70 afslører reguleringsmekanisme, der involverer C-termi…Figur:Under oxidative stressforhold, den molekylære chaperon Hsp70 undergår post-translationel modifikation af cysteinrester ved tilsætning af tripeptidet glutathion. Glutathionylering inden for det s
S-glutathionylering af human-inducerbar Hsp70 afslører reguleringsmekanisme, der involverer C-termi…Figur:Under oxidative stressforhold, den molekylære chaperon Hsp70 undergår post-translationel modifikation af cysteinrester ved tilsætning af tripeptidet glutathion. Glutathionylering inden for det s
- Hvad er en kraft mellem to bevægelige genstande, der berører?
- Hvorfor får månen lys fra solen?
- Forskere bruger uordnet stof til beregning, udviklende banebrydende nanopartikel boolesk logiknetvæ…
- Alle organismer i kongerigerne Protista Animalia Plantae og svampe er?
- Raketudviklingen får et kolossalt løft
- Et materiale, der er superledende ved stuetemperatur og lavere tryk


