Stærke vs. svage syrer og baser:ledningsevne forklaret
Ionernes rolle i elektrisk ledningsevne
* Elektricitet bæres af ladede partikler (ioner). I opløsninger dannes disse ioner, når stoffer opløses og dissocieres (brydes fra hinanden) til deres bestanddele.
* Stærke syrer og baser ioniseres fuldstændigt i opløsning. Det betyder, at de genererer en høj koncentration af frie ioner.
* Svage syrer og baser ioniseres kun delvist i opløsning. De skaber en meget lavere koncentration af frie ioner.
Forbindelsen til ledningsevne
* Høj ionkoncentration =Høj ledningsevne. Jo flere ioner der er til stede i en opløsning, jo lettere er det for en elektrisk strøm at strømme gennem den.
* Lav ionkoncentration =Lav ledningsevne. En løsning med færre ioner giver mere modstand mod strømmen af elektricitet.
Eksempel
* Saltsyre (HCl) er en stærk syre. Når det opløses i vand, opløses det fuldstændigt til H+ og Cl-ioner. Dette skaber en høj koncentration af ioner, hvilket fører til høj ledningsevne.
* Eddikesyre (CH3COOH) er en svag syre. Det ioniserer kun delvist i opløsning og producerer et mindre antal H+ og CH3COO-ioner. Den lavere ionkoncentration resulterer i lavere ledningsevne.
I oversigt
Den vigtigste forskel mellem stærke og svage syrer/baser ligger i deres ioniseringsgrad. Stærke syrer og baser genererer en meget større pulje af frie ioner, hvilket muliggør effektiv elektrisk ledning. Svage syrer og baser producerer med deres begrænsede ionisering færre ioner, hvilket resulterer i dårligere elektrisk ledningsevne.
 Varme artikler
Varme artikler
-
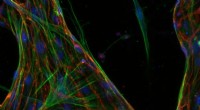 Mikrofluidisk chip kan reducere bivirkninger ved strålebehandlingMikrovaskulaturen (blodkar -systemer i organer) dannet inde i chippen. Kredit:Joe Vittorio Organ-on-a-chip teknologi bruges til at udvikle 3D-modeller, der gør det muligt for forskere i det sydlig
Mikrofluidisk chip kan reducere bivirkninger ved strålebehandlingMikrovaskulaturen (blodkar -systemer i organer) dannet inde i chippen. Kredit:Joe Vittorio Organ-on-a-chip teknologi bruges til at udvikle 3D-modeller, der gør det muligt for forskere i det sydlig -
 Video:Vampyrfolklore har mere kemi, end du trorKredit:The American Chemical Society Halloween -sæsonen ville ikke være den samme uden de udøde. Denne uge om reaktioner, vi pakker den kemi ud, der måske har inspireret en af vores favoritter:
Video:Vampyrfolklore har mere kemi, end du trorKredit:The American Chemical Society Halloween -sæsonen ville ikke være den samme uden de udøde. Denne uge om reaktioner, vi pakker den kemi ud, der måske har inspireret en af vores favoritter: -
 Saturns største måne kan være nøglen til renere motorerTitans atmosfæriske dis, Saturns største måne (billedet her langs Saturns midtersektion), er fanget i dette naturlige farvebillede (boks til venstre). Kredit:NASA Jet Propulsion Laboratory, Space Scie
Saturns største måne kan være nøglen til renere motorerTitans atmosfæriske dis, Saturns største måne (billedet her langs Saturns midtersektion), er fanget i dette naturlige farvebillede (boks til venstre). Kredit:NASA Jet Propulsion Laboratory, Space Scie -
 Udnyttelse af solen til at tackle fattigdomKredit:CC0 Public Domain Et genanvendeligt hygiejnebind, der potentielt kan dræbe op til 99,9% af bakterierne, når det udsættes for sollys, er ved at blive udviklet af forskere ved Cardiff Univers
Udnyttelse af solen til at tackle fattigdomKredit:CC0 Public Domain Et genanvendeligt hygiejnebind, der potentielt kan dræbe op til 99,9% af bakterierne, når det udsættes for sollys, er ved at blive udviklet af forskere ved Cardiff Univers
- Hvad er de fire vigtigste elementer i levende organismer?
- Hvad er en type ny konstellation, som Edmond Halley så på himlen, mens han var på Island St. Hele…
- Hvorfor phenoler, ikke benzoesyre, reagerer med jernklorid for at producere farve
- Kobber-indiumoxid:En hurtigere og køligere måde at reducere vores CO2-fodaftryk
- Hvilket materiale giver varme, selv når det er vådt?
- Hvor mange protoner og Americium har elementet Radium?


