Ionisk ledningsevne i løsning:Forstå ændringen
1. Ioniske forbindelser i fast tilstand:
* Krystallinsk struktur: Ioniske forbindelser eksisterer i en krystallinsk struktur, hvor positivt ladede kationer og negativt ladede anioner er arrangeret i et fast, stift gitter.
* Ingen frie ioner: Ionerne holdes tæt på plads af elektrostatiske kræfter, hvilket forhindrer dem i at bevæge sig frit. Denne mangel på mobile ladningsbærere betyder, at faste ioniske forbindelser er dårlige ledere af elektricitet.
2. Opløsning i vand:
* Polær opløsningsmiddel: Vand er et polært opløsningsmiddel, hvilket betyder, at det har en positiv ende (brint) og en negativ ende (ilt).
* Ion-dipol-interaktioner: De positive ender af vandmolekyler tiltrækkes af anionerne af den ioniske forbindelse, og de negative ender af vandmolekyler tiltrækkes af kationerne.
* Løsning: Disse attraktioner trækker ionerne fra krystalgitteret og omgiver dem med vandmolekyler. Denne proces kaldes solvation.
3. Elektrisk ledningsevne i løsning:
* Fri ioner: Når først den ioniske forbindelse er opløst, er ionerne nu frie til at bevæge sig gennem opløsningen. Disse mobile, ladede arter kan bære elektrisk strøm.
* Øget ledningsevne: Tilstedeværelsen af disse mobile ioner gør løsningen til en god leder af elektricitet. Jo flere ioner til stede, jo højere ledningsevne.
Opsummering:
Nøglefaktoren er bevægelsen af ladningsbærere. Faste ionforbindelser mangler frie ioner, så de er dårlige ledere. Når ionerne er opløst i vand, frigives de og bliver mobile, hvilket fører til betydelige stigninger i elektrisk ledningsevne.
 Varme artikler
Varme artikler
-
 Den komplette guide til udvinding, behandling og forædling af naturgasUdtrækning Naturgasudvinding begynder med boring af en brønd. Disse brønde er specialboret for naturgas, men fordi naturgas ofte findes i de samme forekomster som olie, er naturgasudvinding nogle gan
Den komplette guide til udvinding, behandling og forædling af naturgasUdtrækning Naturgasudvinding begynder med boring af en brønd. Disse brønde er specialboret for naturgas, men fordi naturgas ofte findes i de samme forekomster som olie, er naturgasudvinding nogle gan -
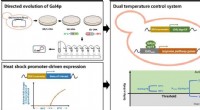 Dobbelt temperaturkontrolsystem til regulering af isoprenbiosyntese i bagegærSkematisk over det dobbelte temperaturkontrolsystem udviklet af Gal4p rettet evolution og ekspressionsregulering til forbedring af isoprenproduktion. Kredit:Jiaxi Lin Bagegær, Saccharomyces cerevis
Dobbelt temperaturkontrolsystem til regulering af isoprenbiosyntese i bagegærSkematisk over det dobbelte temperaturkontrolsystem udviklet af Gal4p rettet evolution og ekspressionsregulering til forbedring af isoprenproduktion. Kredit:Jiaxi Lin Bagegær, Saccharomyces cerevis -
 Lighederne mellem et Van Gogh-maleri og en golfboldKredit:CC0 Public Domain På molekylær skala, der er overraskende ligheder mellem den ydre skal af en golfbold og den hvide oliemaling, som Van Gogh og hans samtidige bruger. I begge tilfælde vekse
Lighederne mellem et Van Gogh-maleri og en golfboldKredit:CC0 Public Domain På molekylær skala, der er overraskende ligheder mellem den ydre skal af en golfbold og den hvide oliemaling, som Van Gogh og hans samtidige bruger. I begge tilfælde vekse -
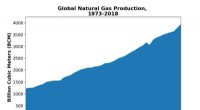 At lave mere af metanGlobal naturgasproduktion over år. Kredit:© 2020-data fra Det Internationale Energiagentur (IEA) Der er fortsat efterspørgsel efter plast og opløsningsmidler fremstillet af petrokemikalier, som ho
At lave mere af metanGlobal naturgasproduktion over år. Kredit:© 2020-data fra Det Internationale Energiagentur (IEA) Der er fortsat efterspørgsel efter plast og opløsningsmidler fremstillet af petrokemikalier, som ho
- Vand er liv:Elfenbenskystens by kæmper med lammende tørke
- Hvorfor danner fluor kun en oxoacid?
- Er aminosyrer en struktur af RNA?
- Facebook fjerner falske italienske konti forud for EU-valget
- Hvad er forholdet mellem gravitation og acceleration på grund af tyngdekraften?
- Hvor mange forskellige energier er der?


