Neutraliseringsreaktioner:Begrænsninger og overvejelser
1. Ufuldstændig neutralisering:
* Svage syrer og baser: Neutraliseringsreaktioner, der involverer svage syrer eller baser, fortsætter ikke til fuldførelse. De når et ligevægtspunkt, hvor en eller anden syre eller base forbliver uomsat. Dette skyldes den begrænsede ionisering af svage syrer og baser.
* Begrænset opløselighed: Hvis saltet dannet i neutraliseringsreaktionen er uopløseligt, vil reaktionen stoppe, når opløsningen bliver mættet med saltet.
2. Sidereaktioner:
* Polyprotiske syrer/baser: Reaktioner, der involverer polyprotiske syrer (som H2SO4) eller polyprotiske baser (som Ca(OH)2) kan resultere i flere neutraliseringstrin, hvilket fører til en mere kompleks reaktionsprofil.
* Hydrolyse af salte: Saltet dannet i en neutraliseringsreaktion kan undergå hydrolyse (reaktion med vand) for at producere sure eller basiske opløsninger, hvilket gør den endelige pH-værdi ikke helt neutral.
3. Temperatureffekter:
* Neutraliseringsvarme: Den varme, der genereres under neutraliseringen, kan forårsage sidereaktioner eller påvirke ligevægten af svage syre/basereaktioner.
* Temperaturafhængighed: Ligevægtskonstanten for neutraliseringsreaktioner kan påvirkes af temperatur, hvilket gør det sværere at forudsige den nøjagtige mængde syre eller base, der kræves til fuldstændig neutralisering.
4. Praktiske overvejelser:
* Urenheder: Prøver fra den virkelige verden kan indeholde urenheder, der kan forstyrre neutraliseringsreaktionen.
* pH-indikatorer: pH-indikatorer, der bruges til at bestemme endepunktet for en neutraliseringsreaktion, er ikke altid præcise og kan føre til fejl ved bestemmelse af det nøjagtige ækvivalenspunkt.
5. Andre faktorer:
* Bufferløsninger: Neutraliseringsreaktioner i bufferopløsninger er mere komplekse, da bufferen modstår pH-ændringer.
* Ikke-vandige opløsningsmidler: Neutraliseringsreaktioner i ikke-vandige opløsningsmidler kan opføre sig anderledes end i vand.
Opsummering:
Neutraliseringsreaktioner er et stærkt værktøj til at forstå syre-base-kemi, men de har begrænsninger, der stammer fra naturen af svage syrer og baser, sidereaktioner og praktiske faktorer. Disse begrænsninger skal tages i betragtning, når neutraliseringsreaktioner anvendes i virkelige omgivelser.
 Varme artikler
Varme artikler
-
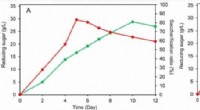 Ny konsolideret bio-saccharificeringsteknik til omdannelse af lignocellulose udvikletForsukring af forbehandlet hvedehalm under optimale eller regelmæssige forhold uden modifikation i både 100-ml anaerobe flasker (a) og en 10-L anaerob fermentor (b). Kredit:LIU Yajun En forskergru
Ny konsolideret bio-saccharificeringsteknik til omdannelse af lignocellulose udvikletForsukring af forbehandlet hvedehalm under optimale eller regelmæssige forhold uden modifikation i både 100-ml anaerobe flasker (a) og en 10-L anaerob fermentor (b). Kredit:LIU Yajun En forskergru -
 Hvordan dannes dis? Sod som en overraskende kilde til dis-opbyggende hydroxylradikalerKredit:© Wiley-VCH Uklarhed dannes, når en cocktail af forskellige gasformige forurenende stoffer oxideres og danner partikler, der spreder sollys. Denne proces er hovedsageligt medieret af hydroxy
Hvordan dannes dis? Sod som en overraskende kilde til dis-opbyggende hydroxylradikalerKredit:© Wiley-VCH Uklarhed dannes, når en cocktail af forskellige gasformige forurenende stoffer oxideres og danner partikler, der spreder sollys. Denne proces er hovedsageligt medieret af hydroxy -
 Forskere på forkant med udvikling af maskinlæringsmetoder til kemisk opdagelseKredit:CC0 Public Domain Opdagelsen og formuleringen af nye lægemidler, antivirale midler, antibiotika og generelt kemikalier med skræddersyede egenskaber er en lang og omhyggelig proces. Tværfa
Forskere på forkant med udvikling af maskinlæringsmetoder til kemisk opdagelseKredit:CC0 Public Domain Opdagelsen og formuleringen af nye lægemidler, antivirale midler, antibiotika og generelt kemikalier med skræddersyede egenskaber er en lang og omhyggelig proces. Tværfa -
 Forskere udvikler værktøjer til at skærpe 3D-visning af store RNA-molekylerUniversity of Maryland forskere udviklede en metode til at udvide omfanget af nuklear magnetisk resonans (NMR) spektroskopi. I eksemplet ovenfor, forskerne var i stand til at skabe et 3D-billede, der
Forskere udvikler værktøjer til at skærpe 3D-visning af store RNA-molekylerUniversity of Maryland forskere udviklede en metode til at udvide omfanget af nuklear magnetisk resonans (NMR) spektroskopi. I eksemplet ovenfor, forskerne var i stand til at skabe et 3D-billede, der
- Hvad er kogepunktet for en frostvæske vandblanding?
- Hvad hedder stjernen, når Nordpolen peger på, da det drejer sig om solen?
- Multigenerationel bolig:En strategi til at klare uoverkommelige boliger?
- Hvilket giver mere energi - et kilo eller uran kul?
- Kosmiske støvpartikler udsætter boble faldskærme på deres brændende nedstigning, opdager forske…
- Hvordan den russiske invasion af Ukraine har påvirket det globale hvedemarked


