Nitrogen-fosforbinding:Forståelse af det kemiske forhold
Her er hvorfor:
* Elektronegativitet: Nitrogen er mere elektronegativt end fosfor. Denne forskel i elektronegativitet gør det usandsynligt for dem at dele elektroner ligeligt i en kovalent binding.
* Valenselektroner: Nitrogen har 5 valenselektroner, mens fosfor har 5. De har begge tendens til at danne tre bindinger for at opnå en stabil oktet. Dette gør det svært for dem at dele elektroner på en måde, der tilfredsstiller begge atomer.
De kan dog interagere indirekte:
* Uorganiske forbindelser: Nitrogen og fosfor kan være en del af den samme uorganiske forbindelse, men de er typisk bundet til andre atomer, ikke direkte til hinanden. For eksempel er nitrogen og phosphor til stede i ammoniumphosphat (NH4)3PO4, men ikke direkte bundet.
* Organiske forbindelser: Nitrogen og fosfor kan være en del af det samme organiske molekyle, men igen, normalt ikke direkte bundet. De kan være forbundet gennem andre atomer, såsom kulstof eller oxygen.
Opsummering: Mens nitrogen og fosfor kan eksistere inden for det samme molekyle, danner de normalt ikke en direkte binding på grund af deres elektronegativitetsforskel og valens.
 Varme artikler
Varme artikler
-
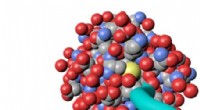 Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl
Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl -
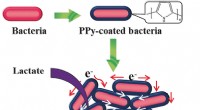 Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s
Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s -
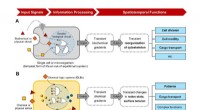 Udforskning af kemiske logiske systemer, der kan reagere på miljøforholdSensing, informationsbehandling og generering af programmerbare funktioner. Skematisk repræsentation af boolsk logik regulerede spatiotemporale funktioner i ude af ligevægt i (A) et levende system (en
Udforskning af kemiske logiske systemer, der kan reagere på miljøforholdSensing, informationsbehandling og generering af programmerbare funktioner. Skematisk repræsentation af boolsk logik regulerede spatiotemporale funktioner i ude af ligevægt i (A) et levende system (en -
 Elektronisk entropi forbedrer vandspaltningKredit:George Hodan/public domain Forskere har længe vidst, at cerium er det bedste element at bruge, når man spalter vand til brint og ilt - en nøgleteknik til at skabe brintgas til brændstof. Me
Elektronisk entropi forbedrer vandspaltningKredit:George Hodan/public domain Forskere har længe vidst, at cerium er det bedste element at bruge, når man spalter vand til brint og ilt - en nøgleteknik til at skabe brintgas til brændstof. Me
- Tata Motors -aktier falder 30% ned på Jaguar -problemer
- Hvor meget kraft kræves for at stoppe en 100 km / h bold den 145 g?
- Hvad hedder sammensat, der udgør de fleste andre gasser?
- Valens og reaktivitet:Sammenligning af elementer med 7 og 8 valenselektroner
- En ballon indeholder en gas med tryk på 580 mm Hg og temperatur 227 grader C Hvad er det nye, når …
- Hvilket materiale accepterer let strømmen af elektroner?


