Forståelse af vands flydende tilstand:Hydrogenbinding forklaret
1. Hydrogenbinding:
* Stærke intermolekylære kræfter: Vandmolekyler er polære, hvilket betyder, at de har en let positiv ende (brintatomer) og en lidt negativ ende (iltatom). Disse modsatte ladninger tiltrækker hinanden og danner stærke brintbindinger mellem molekyler.
* Høj bindingsenergi: Hydrogenbindinger er relativt stærke sammenlignet med andre intermolekylære kræfter som dipol-dipol-interaktioner eller London-spredningskræfter. Denne stærke tiltrækning mellem vandmolekyler kræver en betydelig mængde energi for at bryde, hvilket holder vandet i en flydende tilstand.
2. Bøjet molekylær geometri:
* Polaritet: Vandmolekylets bøjede form bidrager til dets overordnede polaritet, hvilket øger styrken af hydrogenbindinger.
* Høj tæthed: De tætpakkede molekyler på grund af stærk hydrogenbinding giver flydende vand en relativt høj densitet.
3. Temperatur og tryk:
* Smelte- og kogepunkter: De stærke hydrogenbindinger i vand kræver en relativt høj mængde energi at overvinde, hvilket resulterer i højere smelte- og kogepunkter sammenlignet med andre lignende molekyler. Det betyder, at vand forbliver flydende over en lang række temperaturer, der almindeligvis findes på Jorden.
Opsummering: Kombinationen af stærk hydrogenbinding på grund af vands polaritet og bøjede molekylære form, samt dets høje tæthed, resulterer i en flydende tilstand ved stuetemperatur. De stærke intermolekylære kræfter kræver en betydelig mængde energi for at bryde, hvilket fører til dets relativt høje smelte- og kogepunkter.
 Varme artikler
Varme artikler
-
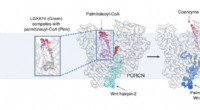 Nye cryo-EM-billeder kaster lys over Wnt-signaleringCryo-EM afslører, hvordan Wnt, et nøglesignalmolekyle for menneskelig udvikling og kræft, modificeres af et enzym ved navn PORCN. Kredit:UT Southwestern Medical Center Ved hjælp af UT Southwesterns
Nye cryo-EM-billeder kaster lys over Wnt-signaleringCryo-EM afslører, hvordan Wnt, et nøglesignalmolekyle for menneskelig udvikling og kræft, modificeres af et enzym ved navn PORCN. Kredit:UT Southwestern Medical Center Ved hjælp af UT Southwesterns -
 Biologer lærte infusoria at bekæmpe giftstofferAntioxidanter modvirker de negative virkninger af brintoverilte på infusorians overlevelse Paramecium caudatum . Det ses, at antioxidanterne øger overlevelsesraten for infusorian i hydrogenperoxidop
Biologer lærte infusoria at bekæmpe giftstofferAntioxidanter modvirker de negative virkninger af brintoverilte på infusorians overlevelse Paramecium caudatum . Det ses, at antioxidanterne øger overlevelsesraten for infusorian i hydrogenperoxidop -
 Belyser usynlige blodige fingeraftryk med en fluorescerende polymerFingeraftryksmønstre fremstillet i blod er tydeligt synlige på aluminiumsfolie (venstre) og malet træ (højre), når de udvikles med en fluorescerende polymer. Kredit:Tilpasset fra ACS Applied Materials
Belyser usynlige blodige fingeraftryk med en fluorescerende polymerFingeraftryksmønstre fremstillet i blod er tydeligt synlige på aluminiumsfolie (venstre) og malet træ (højre), når de udvikles med en fluorescerende polymer. Kredit:Tilpasset fra ACS Applied Materials -
 Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til
Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til
- Toppen af et bjerg nær ækvator er dækket med sne gennem året?
- Borgerforskere sporer stråling syv år efter Fukushima
- Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltning
- Kvantemagasin til mikrobølger
- En bold kastet lodret opad vender tilbage til udgangspunktet på 8 sekunder. Find sin oprindelige ha…
- Er væskerne inde i en celle?


