Salpetersyre og saltreaktion:Forståelse af kemisk uforenelighed
* Salpetersyre er en stærk syre, men det er ikke et stærkt oxidationsmiddel i dette tilfælde. Mens salpetersyre kan fungere som et oxidationsmiddel, er den ikke stærk nok til at oxidere chloridioner (Cl⁻) i salt.
* Natriumioner (Na⁺) er ikke-reaktive. De vil ikke deltage i nogen væsentlig kemisk reaktion med salpetersyre.
Hvad kan der ske:
* Meget fortyndet salpetersyre og salt: Du kan muligvis observere en meget let reaktion, hvor en lille mængde hydrogenchloridgas (HCl) produceres. Dette skyldes, at ligevægten mellem ionerne i opløsning en smule favoriserer dannelsen af HCl, men det er en ubetydelig effekt.
* Koncentreret salpetersyre og varme: Hvis du skulle bruge koncentreret salpetersyre og opvarme blandingen, vil du måske se en mere mærkbar reaktion. Den stærke oxidationsevne af koncentreret salpetersyre kan oxidere chloridioner, hvilket potentielt danner klorgas (Cl₂), som er giftig og har en gullig-grøn farve. Denne reaktion er mere tilbøjelig til at forekomme med varme og ville være et farligt eksperiment.
Opsummering: Reaktionen mellem salpetersyre og salt er ikke en almindelig eller signifikant reaktion under almindelige forhold.
 Varme artikler
Varme artikler
-
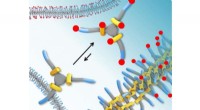 Adhæsiv adfærd af selvkonstruktive materialer målt første gangEt skematisk billede af den nye teknik. De røde prikker repræsenterer deuteriumatomer. Monomererne, der forlader polymeren (afbildet til venstre) vil blive udsat for deuterium i tungt vand, hvilket re
Adhæsiv adfærd af selvkonstruktive materialer målt første gangEt skematisk billede af den nye teknik. De røde prikker repræsenterer deuteriumatomer. Monomererne, der forlader polymeren (afbildet til venstre) vil blive udsat for deuterium i tungt vand, hvilket re -
 Elektrokemi åbner ny adgang til vigtige klasser af stofferEn ung forsker i professor Waldvogels team, der bruger et screeningsapparat til parallel elektrolyseoptimering. Kredit:Alexander Sell Elektrokemi har gennemgået en renæssance i de seneste år, og m
Elektrokemi åbner ny adgang til vigtige klasser af stofferEn ung forsker i professor Waldvogels team, der bruger et screeningsapparat til parallel elektrolyseoptimering. Kredit:Alexander Sell Elektrokemi har gennemgået en renæssance i de seneste år, og m -
 Konstrueret protein inspireret af naturen kan hjælpe med plastikpestMutationer af et PET-hydrolyserende enzym PET2 resulterede i en stigning på 6,7 grader C i termisk stabilitet og en 6,8 gange stigning i PET-hydrolytisk aktivitet. T m repræsenterer smeltetemperatur
Konstrueret protein inspireret af naturen kan hjælpe med plastikpestMutationer af et PET-hydrolyserende enzym PET2 resulterede i en stigning på 6,7 grader C i termisk stabilitet og en 6,8 gange stigning i PET-hydrolytisk aktivitet. T m repræsenterer smeltetemperatur -
 Video:Hvordan drageblod kunne redde dit livKredit:The American Chemical Society Kemikere har fundet potentielle lægemidler og andre virkelig nyttige forbindelser nogle virkelig bizarre steder i naturen. For eksempel, et naturligt immunfor
Video:Hvordan drageblod kunne redde dit livKredit:The American Chemical Society Kemikere har fundet potentielle lægemidler og andre virkelig nyttige forbindelser nogle virkelig bizarre steder i naturen. For eksempel, et naturligt immunfor
- Hvordan en hollandsk mand, der indsamlede affald, endte i en videnskabelig artikel
- ESA udnævner den første astronaut til at flyve på månemissionen Artemis I
- Hvordan kunne et stykke af månen blive en jordnær asteroide? Forskere har et svar
- Har alt et pH-niveau?
- Nye Svalbard-laviner afsløret via satellit
- Hvordan man laver en science fair Poster


