Forståelse af aniondannelse:Hvorfor ikke-metaller har tendens til at få elektroner
Her er hvorfor:
* Elektronegativitet: Ikke-metaller har højere elektronegativitet end metaller. Det betyder, at de har en stærkere tiltrækning af elektroner.
* Elektronkonfiguration: Ikke-metaller har typisk næsten fyldte ydre elektronskaller. At få en eller flere elektroner fuldender deres skal og gør dem mere stabile.
Når ikke-metaller binder sig til metaller, mister metalatomerne elektroner og bliver til kationer (positivt ladede ioner), og ikke-metallerne får disse elektroner til at blive anioner (negativt ladede ioner). Dette resulterer i en ionbinding.
Eksempler på almindelige anioner:
* Halogener: Fluor (F-), Klor (Cl-), Brom (Br-), Jod (I-)
* Oxygen: Oxid (O2-)
* Svovl: Sulfid (S2-)
* Nitrogen: Nitrid (N3-)
Undtagelser:
Mens ikke-metaller generelt danner anioner, er der nogle undtagelser. For eksempel kan brint danne en kation (H+) i nogle forbindelser.
Sidste artikelSur regn:årsager, kilder og miljøpåvirkning - en omfattende guide
Næste artikelAnioner i ionisk binding:Ikke-metallernes rolle
 Varme artikler
Varme artikler
-
 Påvisning af små mængder virus ved tidlige infektionerHøjtryks forkoncentrationsanordninger til at øge styrken af biovæskeprøver, der skal bruges med point-of-care assays til påvisning af patogener, såsom influenza eller coronavirus. Kredit:Amy Drexeli
Påvisning af små mængder virus ved tidlige infektionerHøjtryks forkoncentrationsanordninger til at øge styrken af biovæskeprøver, der skal bruges med point-of-care assays til påvisning af patogener, såsom influenza eller coronavirus. Kredit:Amy Drexeli -
 Forskere skaber en ny elektronegativitetsskalaKredit:Pixabay/CC0 Public Domain Skoltech-kemikere har foreslået en ny elektronegativitetsskala og offentliggjort deres resultater i Naturkommunikation . Begrebet elektronegativitet introducere
Forskere skaber en ny elektronegativitetsskalaKredit:Pixabay/CC0 Public Domain Skoltech-kemikere har foreslået en ny elektronegativitetsskala og offentliggjort deres resultater i Naturkommunikation . Begrebet elektronegativitet introducere -
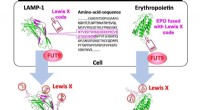 Forskerhold identificerer en molekylær kode indlejret i protein til regulering af dets glykosylerin…Specifik 29-aminosyresekvens fra LAMP-1 tjener som en Lewis X-kode, som dechifreres af FUT9, og den kan indlejres i erythropoietin for at fremkalde Lewis X-modifikation. Kredit:Nagoya City University
Forskerhold identificerer en molekylær kode indlejret i protein til regulering af dets glykosylerin…Specifik 29-aminosyresekvens fra LAMP-1 tjener som en Lewis X-kode, som dechifreres af FUT9, og den kan indlejres i erythropoietin for at fremkalde Lewis X-modifikation. Kredit:Nagoya City University -
 Hvorfor molær masse betyder noget i kemi:En praktisk vejledningAf Jason Thompson, Opdateret 30. august 2022 Når du skal vurdere, hvor meget af et stof du har brug for, kan vægt eller volumen alene være vildledende. Densitetsvariationer betyder, at en tung, kompa
Hvorfor molær masse betyder noget i kemi:En praktisk vejledningAf Jason Thompson, Opdateret 30. august 2022 Når du skal vurdere, hvor meget af et stof du har brug for, kan vægt eller volumen alene være vildledende. Densitetsvariationer betyder, at en tung, kompa
- Hvad er den afbalancerede ligning til reaktion af magnesiummetal og saltsyre?
- Hvad er en imcomplete dominans?
- Hvad er en celle eller en gruppe celler, der er tilstødende kendt som?
- Hvad vi ved om orkanen Irma:fakta, tal, Vejrudsigt
- Ændringer i vandkvaliteten er sat til at lave et sprøjt
- Kvantekryptografi:Gør hacking nytteløst


