Lewis-struktur af CHBr3 (Bromoform):En trin-for-trin guide
1. Tæl valenselektroner:
* Kulstof (C):4 valenselektroner
* Brint (H):1 valenselektron
* Brom (Br):7 valenselektroner hver (3 bromatomer =21 elektroner)
Samlede valenselektroner:4 + 1 + 21 =26
2. Centralatom:
* Kulstof er det mindst elektronegative grundstof, så det vil være det centrale atom.
3. Enkeltobligationer:
* Forbind det centrale carbonatom til brint- og tre bromatomer med enkeltbindinger. Dette bruger 8 elektroner (4 bindinger x 2 elektroner/binding).
4. Resterende elektroner:
* Du har 18 elektroner tilbage (26 - 8).
* Hvert bromatom har brug for 6 elektroner mere for at fuldføre sin oktet (8 valenselektroner).
5. Komplet oktet:
* Placer 3 ensomme elektronpar (6 elektroner hver) rundt om hvert bromatom.
6. Lewis-struktur:
Den endelige Lewis-struktur ser således ud:
```
H
|
Br - C - Br
|
Br
```
Nøglepunkter:
* Kulstofatomet har en komplet oktet med 4 bindinger.
* Hvert bromatom har en komplet oktet med 1 binding og 3 ensomme par.
* Brintatomet har 2 elektroner (en komplet duet).
 Varme artikler
Varme artikler
-
 Sikrere, mere komfortable soldatuniformer er i gangI en test, ubehandlet stof (venstre panel) brænder helt efter en flamme er fjernet, der henviser til, at stof, der er behandlet med fytinsyre (højre panel), er selvslukkende på få sekunder efter, at t
Sikrere, mere komfortable soldatuniformer er i gangI en test, ubehandlet stof (venstre panel) brænder helt efter en flamme er fjernet, der henviser til, at stof, der er behandlet med fytinsyre (højre panel), er selvslukkende på få sekunder efter, at t -
 Stress og belastning:Geokemister besvarer grundlæggende spørgsmål om mineralreaktionerArgonne-forskere brugte kohærent røntgendiffraktionsbilleddannelse til at se på stammen inde i en jernnanopartikel, da den oxiderede. Dette billede viser nanopartiklen gradvist oxiderende. Kredit:Argo
Stress og belastning:Geokemister besvarer grundlæggende spørgsmål om mineralreaktionerArgonne-forskere brugte kohærent røntgendiffraktionsbilleddannelse til at se på stammen inde i en jernnanopartikel, da den oxiderede. Dette billede viser nanopartiklen gradvist oxiderende. Kredit:Argo -
 Afvisende forskning:Søværnet udvikler skibsbelægninger for at reducere brændstof, energiomkostni…Mathew Boban, en kandidatstuderende forskningsassistent ved University of Michigan, hælder hexadecanolie på et objektglas dækket med en omnifobisk belægning. De oliebaserede, meget viskøs olie glider
Afvisende forskning:Søværnet udvikler skibsbelægninger for at reducere brændstof, energiomkostni…Mathew Boban, en kandidatstuderende forskningsassistent ved University of Michigan, hælder hexadecanolie på et objektglas dækket med en omnifobisk belægning. De oliebaserede, meget viskøs olie glider -
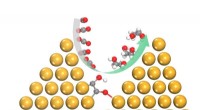 Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
- Hvad er sølvindholdet i et amerikansk nikkel fra 1964?
- NASA-kort giver det mest nøjagtige rumbaserede billede af L.A.s kuldioxid
- Kulilte (CO):Forståelse af carbonatomantal
- Hvordan får du KJ -solenergien i timen?
- Cassini rumfartøj:Forstørrelsesglas ved Saturn indtil slutningen
- Ny MD-simulering kaster lys over mysteriet med hydratiserede elektroners struktur


