Lanthanid-elektronkonfiguration:Hvorfor 5d-elektroner fjernes først
Nøglebegreber
* Energiniveau vs. penetration: Selvom 4f orbitalen faktisk har lavere energi end 5d orbitalen, er den også mere gennemtrængende . Det betyder, at 4f-elektroner bruger mere tid tættere på kernen end 5d-elektroner.
* Afskærmning: 4f elektronerne er skærmet af de fyldte 5s og 5p orbitaler. Dette betyder, at 4f-elektronerne oplever en svagere tiltrækning til kernen sammenlignet med 5d-elektroner.
* Effektiv nuklear ladning: På grund af afskærmning oplever 4f-elektroner en lavere effektiv nuklear ladning end 5d-elektroner.
Forklaringen
1. Lavere energi, men højere penetration: 4f orbitaler er lavere i energi, men har en højere penetration sammenlignet med 5d orbitaler. Dette betyder, at 4f-elektroner er tættere bundet til kernen.
2. Afskærmningseffekt: De fyldte 5s og 5p orbitaler beskytter 4f elektronerne fra kernen, hvilket reducerer deres effektive nukleare ladning.
3. Nemmere fjernelse: 5d-elektronerne, der oplever en stærkere effektiv nuklear ladning på grund af mindre afskærmning, holdes mindre tæt og er dermed lettere at fjerne.
I enklere vendinger:
Forestil dig, at 4f-elektronerne er som en gruppe mennesker, der er samlet tæt på et lejrbål, skærmet mod vinden af en mur. 5d-elektronerne er længere væk, udsat for vinden (repræsenterer kernens træk). Selvom lejrbålet er det samme (repræsenterer energiniveauet), er personerne tættere på bålet (4f elektroner) mere beskyttede og sværere at flytte.
Konsekvenser
Denne effekt forklarer, hvorfor lanthanider har en tendens til at danne ioner med en ladning på +3. Fjernelse af elektroner fra 5d-orbitalen fører først til en relativt stabil konfiguration, og yderligere ionisering bliver stadig sværere på grund af de stramt holdte 4f-elektroner.
Vigtig bemærkning:
Selvom denne forklaring generelt er korrekt, er det vigtigt at huske, at selve ioniseringsprocessen er kompleks og påvirket af mange faktorer. Der er nogle undtagelser, og rækkefølgen af elektronfjernelse er muligvis ikke altid strengt 5d før 4f.
 Varme artikler
Varme artikler
-
 Positive og negative ioner:Hvordan metaller og ikke-metaller danner kationer og anionerAf Carolyn LaRoche, Opdateret 24. marts 2022 Sinhyu/iStock/GettyImages Hvad er en ion? Atomer kan erhverve en elektrisk ladning ved enten at miste eller få elektroner og blive til ioner. En positivt
Positive og negative ioner:Hvordan metaller og ikke-metaller danner kationer og anionerAf Carolyn LaRoche, Opdateret 24. marts 2022 Sinhyu/iStock/GettyImages Hvad er en ion? Atomer kan erhverve en elektrisk ladning ved enten at miste eller få elektroner og blive til ioner. En positivt -
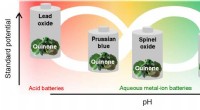 Billig organisk materiale giver sikre batterier en længere levetidUH-forskere har opdaget et nyt materiale, der har vist sig at være en effektiv anode til syre- og alkalibatterier, inklusive nye vandige metal-ion-batterier, giver løftet om sikker, langtidsholdbare b
Billig organisk materiale giver sikre batterier en længere levetidUH-forskere har opdaget et nyt materiale, der har vist sig at være en effektiv anode til syre- og alkalibatterier, inklusive nye vandige metal-ion-batterier, giver løftet om sikker, langtidsholdbare b -
 En ny tilgang til at forbedre katalysatorerne for hydrogenudviklingsreaktionKredit:CC0 Public Domain Et internationalt samarbejde mellem forskere i Spanien og Skotland har resulteret i en ny tilgang til at forbedre de nødvendige katalysatorer til at udføre hydrogenudvikli
En ny tilgang til at forbedre katalysatorerne for hydrogenudviklingsreaktionKredit:CC0 Public Domain Et internationalt samarbejde mellem forskere i Spanien og Skotland har resulteret i en ny tilgang til at forbedre de nødvendige katalysatorer til at udføre hydrogenudvikli -
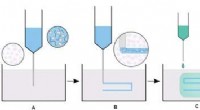 Ny 3-D printteknik til biomaterialerEt skema, der viser produktionen af et 3D bioprintet stillads ved brug af SLAM. A) Væskegel-printlejet skabes ved forskydningsafkøling af en varm agaroseopløsning gennem sol-gel-overgangen, som dere
Ny 3-D printteknik til biomaterialerEt skema, der viser produktionen af et 3D bioprintet stillads ved brug af SLAM. A) Væskegel-printlejet skabes ved forskydningsafkøling af en varm agaroseopløsning gennem sol-gel-overgangen, som dere
- Selvkritisk perfektionisme nager elevernes trivsel allerede i folkeskolen, siger undersøgelse
- Thim Red Rim omkring solen under en solformørkelse kaldes The?
- Ingredienser i sammenføjning Sand
- Hvilken kraft trækker to galakser mod hinanden?
- Højteknologisk sexlegetøj til kvinder vinder en ophævet pris tilbage
- Når en celle bruger kemisk energi til at udføre arbejde, frigives det fra?


